海藻中含丰富的、以离子形式存在的碘元素。下图是实验室从海藻里提取碘的流程的一部分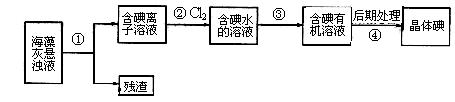
下列判断正确的是
| A.步骤①、③的操作分别是过滤、萃取分液 |
| B.可用淀粉溶液检验步骤②的反应是否进行完全 |
| C.步骤③中加入的有机溶剂是乙醇 |
| D.步骤④的操作是过滤 |
下列实验方案设计正确的是
| A.分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤 |
| B.失去标签的硝酸银溶液、稀盐酸、氢氧化钠溶液、氯化铝溶液,可以用碳酸铵溶液鉴别 |
| C.将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体 |
| D.检验从火星上带回来的红色物体是否是Fe2O3 的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 |
某同学用下列装置验证一些物质的性质。下列说法正确的是
| A.Ⅰ图中:将胶头滴管中的水滴入到金属钠中,能看到U型管左侧红墨水上升 |
| B.Ⅱ图中:观察到湿润的有色布条能褪色,待尾气全部被碱吸收后,将稀硫酸滴入烧杯中,至溶液显酸性,可能看到有黄绿色气体生成 |
| C.Ⅲ图中:观察到量简内黄绿色逐渐消失,量筒内壁有油状物质生成。该现象是由于甲烷与氯气在光照条件下发生了加成反应 |
| D.Ⅳ图中,可以比较KMnO4、Cl2和S还原性的相对强弱 |
甲、 乙、 丙、 丁四种易溶于水的物质,分别由Na+、Ba2+、Al3+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成,已知:
①0.1 mol/L甲溶液中c(H+)>0.1 mol/L;
②将少量乙溶液分别滴入其他三种物质的溶液时,均有白色沉淀生成;
③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。 下列判断正确的是
| A.甲溶液含有SO42- | B.乙溶液含有SO42- |
| C.丙溶液显酸性 | D.丁溶液显酸性 |
下列根据实验操作和现象所得出的结论正确的是:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向溶液中滴加盐酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中不一定含有SO42- |
| B | 向溶液X中先滴加稀NaOH溶液,再将湿润红色石蕊试纸置于试管口附近 | 试纸不变蓝 | 原溶液中无NH4+ |
| C | 向PbO2中滴入浓盐酸 | 有黄绿色气体 | PbO2具有氧化性 |
| D | 向溶液X中加入稀盐酸,并将产生的 无色气体通入澄清石灰水中 | 有白色沉淀生成 | 溶液X中一定含有CO32- |
下列各组物质的无色溶液,不用其他试剂即可鉴别的是( )
①KOH Na2SO4 AlCl3②NaHCO3 Ba(OH)2 H2SO4③HCl NaAlO2 NaHSO4④Ca(OH)2 Na2CO3 BaCl2
| A.①② | B.②③ | C.①③④ | D.①②④ |
下列除去杂质所选用的试剂或方法完全正确的是( )
| A.除去NaCl溶液中的少量I2: 用无水乙醇,萃取分液 |
| B.除 CO2中的少量HCl:通入饱和Na2CO3溶液,洗气 |
| C.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
| D.除去NaHCO3固体中的少量Na2CO3:加热灼烧 |
为使Fe2+,Fe3+,Zn2+较完全地形成氢氧化物沉淀,溶液的酸碱度分别为pH7.7、 pH4.5、pH6.6。某硫酸锌酸性溶液中含有少量Fe2+,Fe3+杂质离子,为除去这些离子制得纯净的ZnSO4,应加入的试剂是( )
| A.H2O2,ZnO | B.氨水 | C.KMnO4,ZnCO3 | D.NaOH溶液 |
现有一块北方盐湖结晶析出的白色晶体.可能含有Na2CO3、Na2SO4、NaCl中的一种 或几种,为了证明其成分,加入试剂的正确顺序为
①加水溶解 ②加入足量的硝酸钡溶液 ③加入足量硝酸 ④加入硝酸银溶液
| A.①④②③ | B.①③②④ | C.④②①③ | D.④③②① |