下列有关操作或判断正确的是( )
| A.配制一定物质的量浓度的溶液时,定容时仰视刻度线会导致所配溶液浓度偏高 |
| B.用托盘天平称取25.20 g NaCl |
| C.用100 mL的量筒量取5.2 mL的盐酸 |
| D.用浓盐酸配制一定物质的量浓度的稀盐酸,量取浓盐酸时仰视量筒的刻度线会导致所配溶液浓度偏高 |
下列有关仪器刻度位置的叙述正确的是
| A.容量瓶容积的刻度线刻在瓶颈上 |
| B.滴定管的“0”标线刻在管的下端 |
| C.托盘天平游码刻度尺的“0”标线刻在尺的右边 |
| D.量筒的最下端刻“0”标线 |
炒河虾由青色变成红色,一同学认为这种红色物质可能是河虾体内某种物质在加热的时候发生颜色的改变。就这位同学的做法而言,这应该属于科学探究步骤中的
| A.实验 | B.观察 | C.假设 | D.分类 |
对以下实验装置图的说法正确的是
| A.利用图①装置做喷泉实验 |
| B.利用图②装置收集SO2并吸收尾气 |
| C.实验室里利用图③装置制取少量纯净的氨气 |
| D.利用图④装置制备氢氧化铁胶体 |
某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )
| A.甲装置:可用来证明碳的非金属性比硅强 |
| B.乙装置:橡皮管的作用是能使水顺利流下 |
| C.丙装置:用图示的方法不能检查此装置的气密性 |
| D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气 |
下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 用铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 溶液中无K+ |
| B | 向溶液中先滴加稀盐酸,再滴加BaCl2溶液 | 先滴加稀盐酸无现象,滴加BaCl2后出现白色沉淀 | 溶液中一定含有SO42- |
| C | 向一定浓度的CuSO4溶液中通入适量H2S气体 | 出现黑色沉淀 | H2S的酸性比H2SO4强 |
| D | 向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无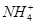 |
下列实验装置设计正确、且能达到目的的是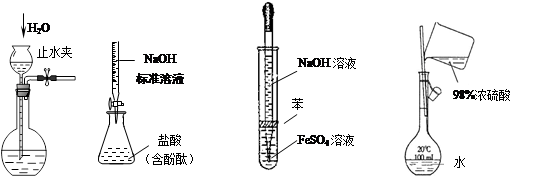
Ⅰ Ⅱ Ⅲ Ⅳ
| A.实验I: 检查装置的气密性 |
| B.实验II:测定未知盐酸的浓度 |
| C.实验III:制取并观察Fe(OH)2沉淀 |
| D.实验IV:配置一定的物质的量浓度的稀硫酸溶液 |
对含微量I-的某样品进行I-化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用Na2S2O3标准溶液滴定以求得I-的浓度。下列分析正确的是
已知:5I-+IO3-+6H+=3H2O+3I2 I-+3Br2(过量)+3H2O=6H++6Br-+IO3-
方法一I-(样品) IO3-
IO3-
 I2
I2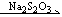 I-
I-
方法二I-(样品) I2
I2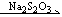 I-
I-
| A.方法二对样品所做处理操作简便,用作微量的测定更准确 |
| B.当待测液由无色变为蓝色时即达到滴定终点 |
| C.方法一与方法二测量出的样品浓度比为6:l |
| D.假设各步骤操作均得当,方法一所消耗Na2S2O3标准溶液的体积是方法二的6倍 |
下列实验与物质微粒大小无直接关系的是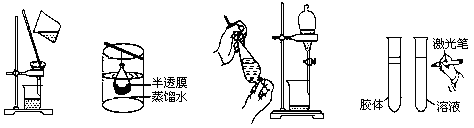
| A.过滤 | B.渗析 | C.萃取 | D.丁达尔效应 |
