碘盐的主要成分是KIO3和NaCl,KIO3在工业上可用电解法制取,以石墨和铁为电极,电解KI溶液,反应方程式为KI+3H2O=KIO3 +3H2↑。下列有关说法中正确的是
| A.电解时,石墨作阴极,铁作阳极 |
| B.电解时,在阴极上产生KIO3 |
| C.电解后电解质溶液pH变大 |
| D.电解中每转移0.6mol e-,理论上可得到0.1mol无水KIO3晶体 |
用a、b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[n(AlCl3):n(CuSO4)=1:9 ]。t1时刻a电极得到混合气体,其中Cl2在标准状况下为 224 mL(忽略气体的溶解);t2时刻Cu全部在电极上析出。下列判断正确的是
| A.a电极与电源的负极相连 |
| B.t2时,两电极的质量相差3.84 g |
| C.电解过程中,溶液的pH不断增大 |
| D.t2时,b电极的电极反应是2H2O-4e-=2OH-+H2↑ |
下列与装置有关的说法正确的是
| A.图a中,随着电解的进行溶液中H+的浓度越来越大 |
| B.图b中,Mg电极作电池的负极 |
| C.图c中,发生的反应为Co+Cd2+= Cd+Co2+ |
| D.图d中:K分别与M、N连接,Fe电极均受到保护不会腐蚀 |
有关下列电化学装置的说法中正确的是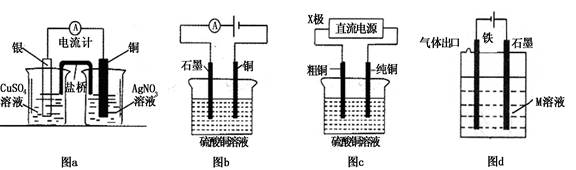
| A.图a是原电池装置,可以实现化学能转化为电能 |
| B.图b电解一段时间后,加入适量CuCO3固体,可以使硫酸铜溶液恢复到原浓度 |
| C.图c中的X极若为负极,则该装置可实现粗铜的精炼 |
| D.图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如右图所示,该装置中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是( )
| A.负极的电极反应式为:CO+O2—―2e-=CO2 |
| B.工作时电极b作正极,O2-由电极a流向电极b |
| C.工作时电子由电极a通过传感器流向电极b |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |
下列说法正确的是
| A.工业上用电解MgCl2溶液的方法制备金属Mg |
| B.在潮湿的空气中,生铁比纯铁更耐腐蚀 |
| C.向鸡蛋清中加入饱和的CuSO4或(NH4)2SO4溶液均产生沉淀,两者原理相同 |
| D.往沸水中滴入饱和的FeCl3溶液,继续煮沸至液体呈透明的红褐色,可制得Fe(OH)3胶体 |
工业上可用软锰矿(主要成分为MnO2)和闪锌矿(主要成分为ZnS)制取干电池中所需的MnO2和Zn,其工艺流程如下:
下列说法正确的是
| A.酸溶时,MnO2作还原剂 | B.可用盐酸代替硫酸进行酸溶 |
| C.原料硫酸可以循环使用 | D.在电解池的阴极处产生MnO2 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是
| A.充电时阳极反应为Zn-2e-+2OH-=Zn(OH)2 |
| B.充电时OH-向阳极移动 |
| C.放电时每转移3mol e-正极有1 mol K2FeO4被氧化 |
| D.充电时,电源的正极应与电池的Zn(OH)2极相连 |
关于如图装置的叙述,不正确的是( )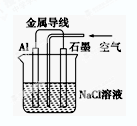
| A.铝是负极,铝片上析出无色气体 |
| B.石墨是正极,石墨棒上析出黄绿色气体 |
| C.溶液中两电极间产生白色沉淀 |
| D.溶液中Na+向石墨方向移动 |
把锌片和铁片放在盛有食盐水和酚酞的混合溶液中(如图所示平面图),一段时间后,两个实验中,先观察到溶液变红的区域是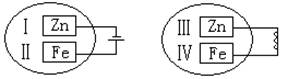
| A.I和III附近 |
| B.I和IV附近 |
| C.II和III附近 |
| D.II和IV附近 |