下图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中正确的是 ( )
| A.A处通入空气,B处通入水煤气 |
| B.a电极的反应式包括:CO+4OH--2e-=CO32-+2H2O |
| C.a电极发生还原反应,b电极发生氧化反应 |
| D.如用这种电池电镀铜,当镀件增重6.4g,则消耗标准状况下的水煤气2.24 L |
MnO2和Zn是制造普通干电池的重要原料,工业上用软锰矿(主要成分MnO2)和闪锌矿(主要成分ZnS)来制取:
①将软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O;
②除去反应混合物中的不溶物;
③电解混合物:MnSO4+ZnSO4+2H2O
 MnO2+Zn+2H2SO4
MnO2+Zn+2H2SO4
下列说法错误的是
| A.干电池是一种将化学能转变为电能的装置 |
| B.步骤③电解时MnO2在阳极处生成,电极反应为:Mn2+-2e-+2H2O=MnO2+4H+ |
| C.步骤①每析出12.8g S沉淀,共转移0.8mol电子 |
| D.步骤③的反应也可以设计成原电池 |
下图为Mg—NaClO燃料电池结构示意图。下列说法正确的是
| A.镁作Y电极 |
| B.电池工作时Na+向负极移动 |
| C.废液的pH大于NaClO溶液的pH |
| D.X电极上发生的反应为:ClO—+2H2O—4e—=ClO3—+4H+ |
工业品氢氧化钾溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。下列说法不正确的是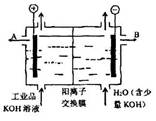
| A.阴极材料可以是Fe,含氧酸根杂质不参与电极上放电 |
| B.该电解槽的阳极反应式为:4OH―― 4e-= 2H2O+O2↑ |
| C.通电后,该电解槽阴极附近溶液pH会减小 |
| D.除去杂质后氢氧化钾溶液从出口B导出 |
电解尿素[ CO(NH2)2]的碱性溶液制氢的装置示意图如图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极)。下列说法正确的是
| A.电解时,b极是阴极放出H2,发生氧化反应 |
| B.溶液中OH—逐渐向b极移动 |
C.电解时,a极的电极反应式为: |
| D.若在b极产生标况下224mL氢气,则消耗尿素2g |
下图所示装置中,a、b、c、d、e、f均为惰性电极,电解质溶液均足量。接通电源后,d极附近显红色。下列说法正确的是
| A.电源B端是正极 |
| B.a、c电极均有单质生成,其物质的量之比为2:1 |
| C.欲用丁装置给铜镀银,N应为Ag,电解液为AgNO3溶液 |
| D.f极附近变红,说明氢氧化铁胶粒带正电荷 |
下图为某太空站的能量转化示意图,其中燃料电池用KOH溶液为电解液。下列说法不正确的是。 
| A.水电解系统中,加入Na2 SO4可增加溶液导电性 |
| B.燃料电池的负极反应:H2+2OH一一2 e一="2" H2O |
| C.整个系统实现了物质零排放及能量间完全转化 |
D.该系统发生总反应:2H2+O2  2 H2O 2 H2O |
下列说法正确的是

| A.图①铜锌原电池工作时,盐桥中的K+移向ZnSO4溶液 |
| B.图②装置反应一段时间,将湿润的KI淀粉试纸靠近碳电极管口,试纸变蓝 |
| C.图③是用海水制取蒸馏水的装置 |
| D.图④装置可用于乙醇提取碘水中的碘 |

