在生产和生活中金属腐蚀难以避免。对图a和图b的分析合理的是
| A.图a,负极上发生的反应是:O2+4e+2H2O → 4OH- |
| B.图b,接通开关后溶液中的H+向正极移动 |
| C.图a,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| D.图b,接通开关后Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
关于下图装置的叙述中正确的是( )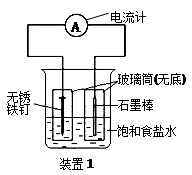
| A.电流由铁钉经过导线流向石墨棒 |
| B.该装置是一个简易的电解饱和食盐水的装置 |
C.石墨棒上发生的电极反应式: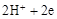 → →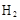 ↑ ↑ |
D.石墨棒上发生的电极反应式: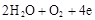 → →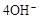 |
关于下图装置中的变化叙述错误的是
| A.电子从锌片流向右侧碳棒,再从左侧碳棒流回铜片 |
| B.锌片上发生氧化反应 |
| C.左侧碳棒上发生:2H2O+O2+4e→4OH- |
| D.铜电极析出铜 |
某兴趣小组设计如下微型实验装置。实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流计A指针偏转。下列有关描述正确的是
A.断开K2,闭合K1时,总反应的离子方程式为:2Cl-+2H+  H2↑+Cl2↑ H2↑+Cl2↑ |
| B.断开K2,闭合K1时,a是电源的正极,铁电极发生氧化反应 |
| C.断开K1,闭合K2时,石墨电极附近溶液变红,铁电极上的电极反应为:Cl2+2e→2Cl- |
| D.断开K1,闭合K2时,石墨电极作正极 |
一种太阳能电池的工作原理如下图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液下列说法不正确的是
| A.K+移向催化剂b |
| B.催化剂a表面发生的化学反应:Fe(CN)64--e- = Fe(CN)63- |
| C.Fe(CN)63-在催化剂b表面被氧化 |
| D.电解池溶液中的Fe(CN)64-和Fe(CN)63-浓度基本保持不变 |
用Pt做电极,电解含C(Cu2+): C(Na+): C(Cl-)=1:2:4的混合溶液,在任何情况下,阴、阳两极下不可能同时发生的反应是
| A.阴极:2H++2e-=H2↑阳极:4OH-- 4e-=2H2O+O2↑ |
| B.阴极:2H++2e-=H2↑阳极:2Cl--2e-=Cl2↑ |
| C.阴极:Cu2++2e-=Cu阳极:4OH-- 4e-=2H2O+O2↑ |
| D.阴极:Cu2++2e-=Cu阳极:2Cl--2e-=Cl2↑ |
一定条件下,碳钢腐蚀与溶液pH的关系如下:
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 |
| 腐蚀快慢 | 较快 | 慢 | 较快 | ||||
| 主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2- | |||
下列说法不正确的是( )
A.在pH<4溶液中,碳钢主要发生析氢腐蚀
B.在pH>6溶液中,碳钢主要发生吸氧腐蚀
C.在pH>14溶液中,碳钢腐蚀的正极反应为O2+4H++4e—=2H2O
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓
原电池与电解池在生活和生产中有着广泛应用。下列有关判断中错误的是
装置① 装置② 装置③
| A.装置①研究的是金属的吸氧腐蚀,Fe上的反应为Fe-2e = Fe2+ |
| B.装置②研究的是电解CuCl2溶液,它将电能转化为化学能 |
| C.装置③研究的是电解饱和食盐水,电解过程中,B极上发生氧化反应 |
| D.三个装置中涉及的主要反应都是氧化还原反应 |
有关下图装置的说法中正确的是
| A.若两电极直接连接,a是食盐水,则发生析氢腐蚀 |
| B.若两电极直接连接,则负极反应一定是:Fe-2e→Fe2+ |
| C.若铁接电源负极,石墨接电源正极,a是食盐水,左侧电极上析出的气泡比右侧电极上的多 |
| D.若铁接电源负极,石墨接电源正极,a是氯化铜,铁上有气泡 |
如图所示,a、b是两根石墨棒。下列叙述正确的是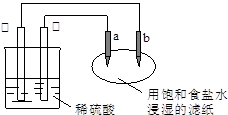
| A.a是正极,发生还原反应 |
| B.b是阳极,发生氧化反应 |
| C.稀硫酸中硫酸根离子的物质的量不变 |
| D.往滤纸上滴加酚酞试液,a极附近颜色变红 |