美国科学家找到了一种突破目前锂离子电池充电量和充电速度限制的方法,该方法将硅簇置入石墨烯层之间,达到提升电池内部锂离子密度的效果,这种材料制成的新型锂电池充电容量和效率都比普通锂电池提高近十倍,下列有关说法正确的是
| A.电池工作时,锂电极为阳极,发生还原反应 |
| B.电池充电时,Li+向阴极移动 |
| C.该电池的化学能可完全转化为电能 |
| D.新材料就是碳和硅化合而成的碳化硅材料 |
关于下图电化学装置中的电极名称、材料及反应均可能正确的是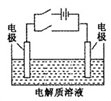
| A.阴极(Cu片)2C1――2e-=Cl2↑ |
| B.正极(石墨棒):Fe3+ +e-= Fe2+ |
| C.阳极(Cu片):4OH――4e-=2H2O+O2↑ |
| D.负极(Fe钉):Fe-3e-=Fe3+ |
用酸性氢氧燃料电池为电源进行电解的实验装置如下图所示。下列说法正确的是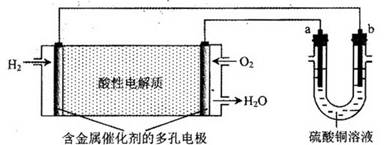
| A.燃料电池工作时,正极反应为:O2+2H2O+4e-=4OH- |
| B.若a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.若a、b极都是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
| D.若a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
某充电电池的原理如图所示,溶液中c(H+)="2.0" mol·L-1,阴离子为SO42-,a、b均为惰性电极,充电时右槽溶液颜色由绿色变为紫色。下列对此电池叙述正确的是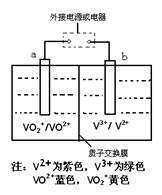
| A.放电过程中,左槽溶液颜色由黄色变为蓝色 |
| B.充电时,b极接直流电源正极,a极接直流电源负极 |
| C.充电过程中,a极的反应式为:VO2++2H++e—= VO2+ +H2O |
| D.放电时,当转移1.0 mol电子时共有1.0 mol H+从左槽迁移进右槽 |
关于下列各装置图的叙述不正确的是
① ② ③ ④
| A.用图①装置精炼铜,a极为粗铜,b为精铜,电解质溶液为CuSO4溶液 |
| B.图②装置的盐桥中KCl的Cl—移向乙烧杯 |
| C.图③装置中钢闸门应与外接电源的负极相连获得保护 |
| D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同 |
已知空气—锌电池的电极反应为:
锌片:Zn+2OH――2e-=ZnO+H2O;碳棒: O2+H2O+2e- =2OH- ,据此判断锌片是
O2+H2O+2e- =2OH- ,据此判断锌片是
| A.正极,被还原 | B.正极,发生还原反应 |
| C.负极,被还原 | D.负极,发生氧化反应 |
电浮选凝聚法处理酸性污水的工作原理如图。下列说法不正确的是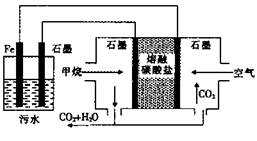
| A.铁电极的电极反应式为:Fe—2e—=Fe2+ |
| B.通人甲烷的石墨电极的电极反应式为:CH4+4CO32——8e—=5CO2+2H2O |
| C.为增强污水的导电能力,可向污水中加人适量工业用食盐 |
| D.若左池石墨电极产生44.8L气体,则消耗0. 5 mol甲烷 |
利用下图密封装置进行实验,起初a、b两处液面相平,放置一段时间。下列说法正确的是
| A.a中发生析氢腐蚀,b中发生吸氧腐蚀 |
| B.一段时间后,a中液面低于b中液面 |
| C.a中溶液的pH增大,b中溶液的pH减小 |
| D.a、b中负极的电极反应式均为Fe-2e-=Fe2+ |
 2Ni(OH)2。根据此反应式,下列 有关说法中正确的是:
2Ni(OH)2。根据此反应式,下列 有关说法中正确的是:  ⑶生产普通玻璃和硅酸盐水泥所需用到的共同原料是 ,导电塑料可表示为
⑶生产普通玻璃和硅酸盐水泥所需用到的共同原料是 ,导电塑料可表示为 ,它属于 材料(填序号)
,它属于 材料(填序号)