锌、铁、镁、铝、锂等金属都可以用在金属燃料电池中,电池的基本结构如图所示。下列说法正确的是
| A.电池工作时,电子沿M→电解液→Y电极流动 |
| B.若M为铝,溶液的pH将不断变大 |
| C.若M为镁,电池总的化学方程式为2Mg+O2=2MgO |
| D.若M为铁,则负极的电极反应式为Fe—2e—=Fe2+ |
电解加工是利用电解原理使金属在电解液中溶蚀成预定形状的方法。电解加工一铜构件的示意图如下:
阳极铜件被溶蚀,而阴极的质量和形状都保持不变,则原始电解液不宜含有大量的
| A.SO42— | B.Cl— | C.Na+ | D.Cu2 + |
以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是 
| A.电池放电时Na+从b极区移向a极区 |
| B.每消耗3 mol H2O2,转移的电子为3 mol |
| C.电极a采用MnO2,MnO2既作电极材料又有催化作用 |
| D.该电池的负极反应为:BH4-+8OH--8e-=BO2-+6H2O |
用如图所示装置进行实验,下列叙述不正确的是
| A.K与N连接时,铁被腐蚀 |
| B.K与N连接时,石墨电极产生气泡 |
| C.K与M连接时,一段时间后溶液的pH增大 |
| D.K与M连接时,石墨电极反应:4OH——4e—==2H2O+O2↑ |
如下图所示,甲池的总反应式为:N2H4+O2=N2+2H2O
下列关于该电池工作时说法正确的是
| A.甲池中负极反应为:N2H4-4e-=N2+4H+ |
| B.甲池溶液pH不变,乙池溶液pH减小 |
| C.甲池中消耗2.24L O2,此时乙池中理论上最多产生12.8g固体 |
| D.反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度 |
下图中X、Y分别是直流电源的两极,通电后,发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的是
| | a极板 | b极板 | X电极 | Z溶液 |
| A | 银 | 铁 | 正极 | AgNO3 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 锌 | 石墨 | 负极 | CuSO4 |
| D | 铜 | 石墨 | 负极 | CuCl2 |
镁燃料电池作为一种高能化学电源,具有良好的应用前景。下图是镁一空气燃料电池工作原理示意图。下列有关该电池的说法正确的是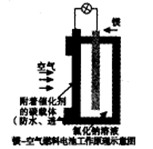
| A.该电池Mg作负极,发生还原反应 |
B.该电池的正极反应式为: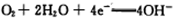 |
| C.电池工作时,电子通过导线由碳电极流向Mg电极 |
| D.当电路中通过0.2mol电子时,消耗的O2体积为1.12L |


