把甲、乙、丙、丁四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若甲、乙相连,甲为负极;丙、丁相连,丁上有气泡逸出;甲、丙相连,甲上发生氧化反应;乙、丁相连,乙是电子流入的一极。则四种金属的活泼性顺序由大到小排列为( )
| A.甲>乙>丙>丁 | B.甲>丙>乙>丁 |
| C.甲>丙>丁>乙 | D.乙>丁>丙>甲 |
在用Zn片、Cu片和稀硫酸组成的电池装置中,下列有关说法不正确的是( )
| A.该装置将化学能转变为电能 | B.溶液中的阴离子向锌电极移动 |
| C.Cu极上有气泡产生,发生还原反应 | D.电流方向是从锌片流向铜片 |
已知空气-锌电池的电极反应为:锌片:Zn+2OH--2e-=ZnO+H2O
石墨:O2 + 2H2O + 4e-=4OH- 根据此判断,锌片是:( )
| A.负极,并被还原 | B.负极,并被氧化 |
| C.正极,并被氧化 | D.正极,并被还原 |
下图是氢氧燃料电池构造示意图。下列说法不正确的是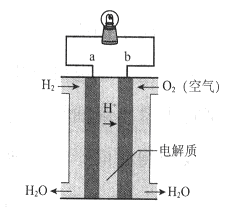
| A.a极是负极 |
| B.电子由b通过灯泡流向a |
| C.该电池总反应是2H2+ O2= 2H2O |
| D.该装置可将化学能转化为电能 |
某同体酸燃料电池以Ca(HSO4)2固体为电解质传递H+,其基本结构如图所示,电池总反应可表示为:2H2+O2=2H2O,下列有关说法错误的是
| A.电子通过外电路从a极流向b极 |
| B.b极上的电极反应式为:O2+4H++4e-=2H2O |
| C.每转移0.4 mol电子,生成3.6g水 |
| D.H+由b极通过固体酸电解质传递到a极 |
下图所示各种装置中能构成原电池的是
| A.①②③ | B.④⑤⑥ | C.①③⑤ | D.②④⑥ |
固体离子导体依靠离子迁移传导电流,Ag+离子可以在RbAg4I5晶体中迁移。下图是一种固体电池。空气中的O2透过聚四氟乙烯膜与AlI3反应生成I2,Ag和I2作用形成原电池。下列说法中错误的是
| A.I2在石墨上被还原 |
| B.石墨电极为负极,银电极为正极 |
| C.Ag+从负极向正极移动 |
| D.银电极的电极反应是:Ag - e— =Ag+ |
下列叙述正确的是
| A.纯锌与稀硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 |
| B.甲醇和氧气以及KOH溶液构成的新型燃料电池中,其负极上发生的反应为:CH3OH+6OH-+6e-=CO2↑+5H2O |
| C.在铁上镀铜时,金属铜作阴极 |
| D.电解MgCl2溶液可制得Mg单质 |
图中,两电极上发生的电极反应为:a极:Cu2++2e—=Cu ,b极:Fe—2e一=Fe2+,下列说法中不正确的是( )
| A.该装置可能是电解池 |
| B.a极上发生的是还原反应 |
| C.a、b不可能是同种电极材料 |
| D.该装置工作时,溶液中的阴离子向b极移动 |
金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+) ( )
| A.阳极发生还原反应,其电极反应式:Ni2++2e-= Ni |
| B.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+ |
| C.电解过程中,阳极质量的减少与阴极质量的增加不相等 |
| D.电解后,电解槽底部的阳极泥中只有Pt |