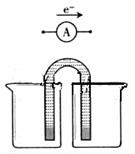
已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH +2H2O  Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是( )
Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是( )
| A.充电过程是化学能转化为电能的过程 |
| B.充电时阳极反应:Ni(OH)2-e- + OH-=" NiOOH" + H2O |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
燃料电池是燃料(例如CO、H2、CH4等)跟氧气或空气反应,将此反应的化学能转化为电能的装置,电解质通常是KOH溶液,则下列关于甲烷燃料电池的说法正确的是( )
| A.负极反应式为:CH4+10OH--8e-=CO32-+7H2O |
| B.正极反应式为:O2+4H++4e-=2H2O |
| C.随着反应地进行,KOH溶液物质的量浓度不变 |
| D.该电池的总反应与甲烷燃烧的反应方程式相同,反应式为:CH4+2O2=CO2+2H2O |
如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置。则下列说法正确的是( )
| A.甲装置中锌为负极,发生还原反应 |
| B.甲装置盐桥的作用是使反应过程中ZnSO4溶液和CuSO4溶液保持电中性 |
| C.乙装置中铁极为阳极,电极反应式为: 2Na++2e-=2Na |
| D.乙装置中B是氯气出口,A是钠出口 |
下面各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )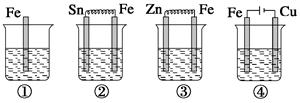
| A.②>①>③>④ | B.④>②>①>③ |
| C.④>②>③>① | D.③>②>④>① |
SO2通过下列工艺流程可制化工业原料H2SO4和清洁能源H2。
下列说法中正确的是
| A.电解槽中也可以用铁电极代替石墨作为阳极 |
| B.原电池中负极的电极反应为:SO2+2H2O+4e-=SO42-+4H+ |
| C.该工艺流程用总反应的化学方程式表示为:SO2+Br2+2H2O=2HBr+H2SO4 |
| D.该生产工艺的优点Br2被循环利用,原电池产生的电能可充分利用,还能获得清洁能源 |
某固体燃料电池以固体氧化铝——氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a.b均不参与电极反应。下列判断不正确的是
| A.在电池内部氧离子(O2-)向负极移动 |
| B.b极对应的电极反应式为:C3H8+10O2-—20e-=3CO2+4H2O |
| C.该电池的总反应方程式为:C3H8+5O2=3CO2+4H2O |
| D.用该电池做电源电解CuSO4溶液时,每消耗1molC3H8时理论上能得到Cu的最大量为5mol |
关于下列装置说法正确的是 
| A.装置①中,盐桥中的K+移向ZnSO4溶液 |
| B.装置②工作一段时间后,a极附近溶液的pH增大 |
| C.用装置③精炼铜时,c极为粗铜 |
| D.装置④中电子由Zn流向Sn,Sn为正极有气泡生成 |