要在铁制品上镀上一定厚度的锌层,以下设计方案正确的是( )
| A.锌作阳极,铁制品作阴极,溶液含有锌离子 |
| B.铂作阴极,铁制品作阳极,溶液含有锌离子 |
| C.铁作阳极,铁制品作阴极,溶液含有亚铁离子 |
| D.锌用阴极,铁制品作阳极,溶液含有锌离子 |
下列有关金属腐蚀与防护的说法正确的是( )
| A.生铁比软铁芯(几乎是纯铁)更不容易生锈 |
| B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护船壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
“天宫一号”飞行器白天靠太阳能帆板产生电流向镍氢电池充电,夜间镍氢电池向飞行器供电。镍氢电池结构示意图如图。若电池总反应为:Ni(OH)2  NiOOH+1/2H2,充电时阴极反应为:H2O+e-=1/2H2+OH-。则下列说法正确的是( )
NiOOH+1/2H2,充电时阴极反应为:H2O+e-=1/2H2+OH-。则下列说法正确的是( )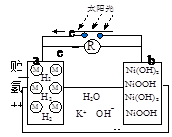
| A.充电时a极为正极 |
| B.放电时NiOOH发生氧化反应 |
| C.充电时,OH-向移a极, K+移向b极 |
| D.放电时正极反应为:NiOOH + H2O +e- = Ni(OH)2 + OH- |
关于下列各图的说法,正确的是( )
| A.①中阴极处能产生使湿润淀粉KI试纸变蓝的气体 |
| B.②中待镀铁制品应与电源正极相连 |
| C.③中电子由b极流向a极 |
| D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
关于下列各装置图的叙述中,正确的是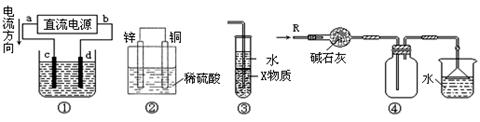
| A.若采用装置①精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
| B.装置②是原电池,能将化学能转化为电能,锌电极发生还原反应 |
| C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
| D.装置④可用于收集氨气,并吸收多余的氨气 |
热激活电池可用作火箭、导弹的工作电源。其基本结构如图所示,作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池的总反应方程式为:
PbSO4+2LiCl+Ca CaCl2+Li2SO4+Pb。下列有关说法正确的是( )
CaCl2+Li2SO4+Pb。下列有关说法正确的是( )
A.正极反应式:Ca+2Cl--2e- CaCl2 CaCl2 |
| B.常温时,在正负极间接上电流表或检流计,指针不偏转 |
| C.放电过程中,Li+向负极移动 |
| D.每转移0.1 mol电子,理论上生成20.7 g Pb |
市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。她的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传到Li+的高分子材料。这种锂离子电池反应式为:Li + 2Li0.35NiO2=" 2" Li0.85NiO2
下列说法不正确的是 ( )
| A.放电时,负极的电极反应式:Li -e- = Li+ |
| B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应 |
| C.该电池不能用水作为电解质 |
| D.放电过程中Li+ 向负极移动 |
关于如图所示装置的叙述,正确的是( )
| A.铜是阳极,铜片上有气泡产生 | B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 | D.氢离子在铜片表面被还原 |
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
| A.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B.脱氧过程中铁作原电池正极,电极反应为:Fe – 3e– = Fe3+ |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O + O2 + 4e–= 4OH– |
| D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
如图所示,将铁棒和石墨棒插入饱和食盐水中。下列说法正确的是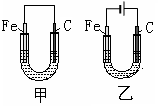
| A.甲中铁被保护不会腐蚀 |
| B.甲中正极反应式为4OH--4e- = 2H2O+O2 |
| C.乙中铁电极上发生氧化反应 |
| D.乙中石墨电极附近滴几滴碘化钾淀粉溶液变蓝色 |