用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示, 则下列 有关说法中不正确的是( )
| A.X为直流电源的负极,Y为直流电源的正极 |
| B.阳极区pH增大 |
| C.图中的b>a |
| D.该过程中的产品主要为H2SO4和H2 |
市场上经常见到的标记为Li-ion的电池。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应式为: Li+2Li0.35NiO2  2Li0.85NiO2,下列说法不正确的是( )
2Li0.85NiO2,下列说法不正确的是( )
| A.放电时,负极的电极反应式:Li-e-=Li+ |
| B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应 |
| C.该电池既能用酸溶液又能用碱溶液作电解质溶液。 |
| D.放电过程中Li+向正极移动 |
如图是一种可充电的锂离子电池充放电的工作示意图。放电时该电池的电极反应式为:负极:LixC6-xe-=C6+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料)正极:Li1-xMnO2+xLi++xe-=LiMnO2(LiMnO2表示含锂原子的二氧化锰)。下列有关说法正确的是 ( )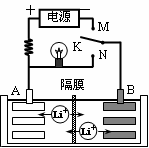
| A.在整个充、放电过程中至少存在3种形式的能量转化 |
| B.K与M相接时,A是阴极,发生还原反应 |
| C.K与N相接时,Li+由A极区迁移到B极区 |
D.该电池的总反应式为Li1-xMnO2+LixC6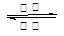 LiMnO2+C6 LiMnO2+C6 |
被称之为“软电池”的纸质电池,其电池总反应为Zn+2MnO2+H2O ZnO+2MnO(OH)。下列说法正确的是( )
ZnO+2MnO(OH)。下列说法正确的是( )
| A.该电池的正极为锌 |
| B.该电池反应中二氧化锰起催化剂作用 |
| C.当65 g Zn完全溶解时,流经电极的电子为1mol |
D.电池正极反应式为2MnO2+2e-+2H2O 2MnO(OH)+2OH- 2MnO(OH)+2OH- |
将如图所示实验装置的K闭合,下列判断正确的是( )
A.电子沿Zn a a b b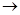 Cu路径流动 Cu路径流动 |
| B.片刻后可观察到滤纸b点变红色 |
| C.片刻后甲池中c(SO42-)增大 |
D. 电极上发生还原反应 电极上发生还原反应 |
不能用Fe+H2SO4=FeSO4+H2↑表示的是( )
| A.用导线将铁片和铜片连接后,放入一盛有稀 H2SO4溶液的烧杯中 |
| B.将铁片直接放入一盛有稀 H2SO4溶液的烧杯中 |
| C.Cu片作阳极,铁片作阴极,电解一定量的H2SO4溶液 |
| D.Cu片作阴极,铁片作阳极,电解一定量的H2SO4溶液 |
理论上不能设计为原电池的化学反应是( )
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(1);△H<0 |
| B.HNO3(1)+NaOH(1)=NaNO3(1)+H2O(1);△H<0 |
| C.2H2(g)+O2(g)=2H2O(1);△H<0 |
| D.2FeCl3(1)+Fe(s)=3FeCl2(1);△H<0 |
在钢铁的电化腐蚀中,正极上发生的反应可能是
| A.Fe - 2e—=Fe2+ | B.O2+4e-+2H2O=4OH- |
| C.4OH- - 4e-=O2↑+2H2O | D.4Fe(OH)2+O2+2H2O =4Fe(OH)3 |
下列事实解释准确的是
| A.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。脱氧过程中铁作原电池正极,电极反应为: Fe-2e- = Fe2+ |
| B.酸性氢氧燃料电池的正极电极反应为: 2H2O十O2+4e-=4OH- |
| C.用石墨电极电解CuC12溶液:阳极上发生的反应:2C1-—2e一=C12↑ |
| D.铅蓄电池的正极反应为:PbO2 +4H+ +2e一=Pb2+ +2H2O |