碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。以下说法正确的是 ( )。
| A.电池工作时,MnO2失去电子 |
| B.电池工作时,电子由锌经外电路流向MnO2 |
| C.从反应方程式来看,不使用氢氧化钾,也不影响电流大小 |
| D.电池的正极反应式为2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq) |
某种聚合物锂离子电池放电时的反应为Li1-xCoO2+LixC6=6C+LiCoO2,其电池如图所示。下列说法不正确的是 ( )。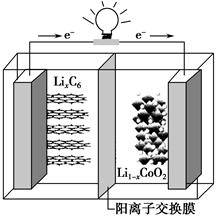
| A.放电时,LixC6发生氧化反应 |
| B.充电时,Li+通过阳离子交换膜从左向右移动 |
| C.充电时将电池的负极与外接电源的负极相连 |
| D.放电时,电池的正极反应为Li1-xCoO2+xLi++xe-=LiCoO2 |
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是 ( )。
| A.X为直流电源的正极,Y为直流电源的负极 |
| B.阴极的电极反应式为2H++2e-=H2↑ |
| C.该过程中的产品主要为H2SO4和H2 |
| D.图中的b>a |
甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能。乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水。下列说法中不正确的是 ( )。
| A.装置乙的a极要与装置甲的X极连接 |
| B.装置乙中b极的电极反应式为2Cl--2e-=Cl2↑ |
| C.若有机废水中主要含有葡萄糖,则装置甲中M极发生的电极应为C6H12O6+6H2O-24e-=6CO2↑+24H+ |
| D.N电极发生还原反应,当N电极消耗5.6 L(标准状况下)气体时,则有2NA |
CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法中错误的是 ( )。
| A.负极的电极反应式为CO+O2--2e-=CO2 |
| B.工作时电极b作正极,O2-由电极a向电极b移动 |
| C.工作时电子由电极a通过传感器流向电极b |
| D.传感器中通过的电流越大,尾气中CO的含量越高 |
能够使反应Cu+2H2O=Cu(OH)2+H2↑发生的是( )
| A.铜片作原电池的负极,碳棒作原电池的正极,氯化钠作电解质溶液 |
| B.铜锌合金在潮湿的空气中发生电化学腐蚀 |
| C.用铜片作阴、阳电极,电解硫酸钠水溶液 |
| D.用铜片作阴、阳电极,电解硫酸铜水溶液 |
下列叙述中不正确的是( )
| A.电解池的阳极上发生氧化反应,阴极上发生还原反应 |
| B.原电池的正极上发生氧化反应,负极上发生还原反应 |
| C.电镀时,电镀池里的阳极材料发生氧化反应 |
| D.用原电池做电源进行电解时,电子从原电池负极流向电解池阴极 |
下图是某同学设计的原电池装置,下列叙述中正确的是( )。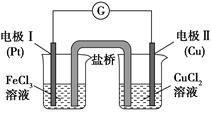
| A.电极Ⅰ上发生还原反应,做原电池的正极 |
| B.电极Ⅱ的电极反应式为Cu2++2e-=Cu |
| C.该原电池的总反应式为2Fe3++Cu=Cu2++2Fe2+ |
| D.盐桥中装有含氯化钾的琼脂,其作用是传递电子 |
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O电解,Al2O3+3H2↑
电解过程中,以下判断正确的是 ( )。
| | 电池 | 电解池 |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3 mol Pb | 生成2 mol Al2O3 |
| C | 正极:PbO2+4H++2e-=Pb2++2H2O | 阳极:3Al+3H2O-6e-=Al2O3+6H+ |
| D |  |  |
