电化学在日常生活中用途广泛,图①是镁次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图②是Cr2O72-的工业废水的处理。下列说法正确的是( )
| A.图②中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| B.图②的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生 |
| C.图①中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓ |
| D.若图①中3.6 g镁溶解产生的电量用于图②废水处理,理论可产生10.7 g氢氧化铁沉淀 |
RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。图为RFC工作原理示意图,下列有关说法正确的是( )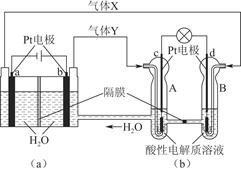
| A.图(a)把化学能转化为电能,图(b)把电能转化为化学能,水得到了循环使用 |
| B.当有0.1 mol电子转移时,a极产生0.56 L O2(标准状况下) |
| C.c极上发生的电极反应是:O2+4H++4e-=2H2O |
| D.图(b)中电子从c极流向d极,提供电能 |
图甲中电极均为石墨电极,下列叙述中正确的是( )
| A.电子沿a→d→c→d路径流动 |
| B.b极的电极反应为O2+4e-+4H+=2H2O |
C.通电初期乙中的总反应为Cu+H2SO4 CuSO4+H2↑ CuSO4+H2↑ |
| D.反应过程中,甲、乙装置中溶液的pH都逐渐减小 |
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯化铝锂(LiAlCl4)溶解在亚硫酰氯(SOClCl)中形成的,其电池总反应方程式为8Li+3SOCl2=6LiCl+Li2SO3+2S。下列叙述中正确的是( )
| A.电解质溶液可以用水,也可以用饱和食盐水 |
| B.电池工作过程中,亚硫酰氯(SOCl2)被还原成Li2SO3 |
| C.电池工作时,锂电极为正极,石墨电极为负极 |
| D.电池工作过程中,金属锂提供的电子与正极区析出的硫的物质的量之比为4∶1 |
科学家们在研制一种吸气式的锂—空气电池,工作时吸收空气中的氧气在多孔金制成的正极表面上反应。总反应可表示为2Li+O2 Li2O2,下列有关说法正确的是( )
Li2O2,下列有关说法正确的是( )
| A.充电时,多孔金制成的电极外接电源负极 |
| B.放电时,吸收空气中22.4 L的O2,就有2 mol e-从电池负极流出 |
| C.放电时,Li+从负极向正极移动 |
| D.该电池可使用含Li+的水溶液作电解质溶液 |
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体。Fe(OH)3有吸附性,可吸附污物使之沉积下来,具有净化水的作用。模拟处理装置如图所示,下列说法错误的是( )
A.X电极是负极,电极反应式为CH4-8e-+4CO32-=5CO2+2H2O |
| B.铁作阳极,失去电子生成Fe2+ |
| C.工作时熔融盐中的碳酸根移向Y电极 |
| D.污水中存在反应4Fe2++10H2O+O2=4Fe(OH)3↓+8H+ |
肼(N2H4)—空气燃料电池是一种环保型碱性燃料电池,电解质为20%~30%的KOH溶液,电池总反应为N2H4+O2=N2+2H2O。下列关于该电池工作时说法中正确的是( )
| A.正极的电极反应式:O2+4H++4e-=2H2O |
| B.溶液中的阴离子向正极移动 |
| C.负极的电极反应式:N2H4+4OH--4e-=4H2O+N2 |
| D.溶液的pH保持不变 |
根据图所示装置,下列说法不正确的是( )
| 选项 | 开关状态 | 溶液A | 电极B | 说明 |
| A | 打开K1,闭合K2 | NaCl | 石墨 | 正极反应:O2+2H2O+4e-=4OH- |
| B | 打开K1,闭合K2 | NaCl | Zn | 铁制品保护:牺牲阳极的阴极保护法 |
| C | 打开K2,闭合K1 | CuSO4 | Cu | 铁表面镀铜 |
| D | 打开K2,闭合K1 | CuSO4 | 粗铜 | 电解法精炼铜 |
1966年美国福特汽车公司首次发表了Na-S电池的有关报导。其结构如图所示,电池反应为2Na+ S8
S8 Na2Sn。下列说法不正确的是
Na2Sn。下列说法不正确的是
| A.熔钠电极作电池的正极 |
| B.放电时Na+向正极移动 |
| C.充电时熔钠电极与电源的负极相连 |
| D.充电时阳极反应式为8Sn2-—16e-=nS8 |
热激活电池可用作火箭、导弹的工作电池。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池的总反应方程式为:PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb。下列有关说法正确的是( )
|
C.每转移0.1mol电子,理论上生成20.7gPb
D.正极反应式:Ca +2Cl--2e-=CaCl2