如图中,两电极上发生的电极反应如下: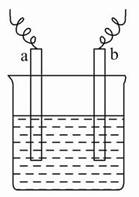
a极:Cu2+ + 2e-=Cu;
b极:Fe-2e-=Fe2+,则以下说法中不正确的是( )
| A.该装置一定是原电池 |
| B.a极上一定发生还原反应 |
| C.a、b可以是同种电极材料 |
| D.该过程中能量的转换可以是电能转化为化学能 |
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
| A.未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程 |
| B.因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |
| C.电镀时保持电流恒定,升高温度不改变电解反应速率 |
| D.镀锌层破损后对铁制品失去保护作用 |
用电解法提取氯化铜废液中的铜,方案正确的是( )
| A.用铜片连接电源的正极,另一电极用铂片 |
| B.用碳棒连接电源的正极,另一电极用铜片 |
| C.用氢氧化钠溶液吸收阴极产物 |
| D.用带火星的木条检验阳极产物 |
如图是模拟电化学反应装置图。下列说法正确的是( )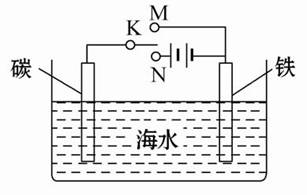
| A.开关K置于N处,则铁电极的电极反应式为:Fe-2e-=Fe2+ |
| B.开关K置于N处,可以减缓铁的腐蚀 |
| C.开关K置于M处,则铁电极的电极反应式为: 2Cl--2e-=Cl2↑ |
| D.开关K置于M处,电子从碳棒经开关K流向铁棒 |
如图所示是探究铁发生腐蚀的装置图。发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升。下列说法中不正确的是( )
| A.开始时发生的是析氢腐蚀 |
| B.一段时间后发生的是吸氧腐蚀 |
| C.两种腐蚀负极的电极反应式均为Fe-2e-=Fe2+ |
| D.析氢腐蚀的总反应式为2Fe+O2+2H2O=2Fe(OH)2 |
下列有关金属保护方法的说法中正确的是( )
| A.我们使用的快餐杯表面有一层搪瓷,搪瓷层破损后仍能起到防止铁生锈的作用 |
| B.白铁(镀锌铁)镀层破损后,铁皮的腐蚀速率很慢 |
| C.轮船的船壳水线以下常装有一些锌块,这是利用了牺牲阴极的阳极保护法 |
| D.钢铁制造的暖气管道外常涂有一层沥青,这是钢铁的电化学保护法 |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2
下列有关该电池的说法不正确的是( )
| A.电池的电解液为碱性溶液,正极为Ni2O3,负极为Fe |
| B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| C.电池充电过程中,阴极附近溶液的pH降低 |
| D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
某铅酸蓄电池的工作原理如图所示,其总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。下列判断不正确的是( )
| A.闭合K时,d电极的反应式为PbSO4+2H2O-2e-=PbO2+4H++SO42— |
| B.当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol |
| C.闭合K时,Ⅱ中SO42—向c电极迁移 |
| D.闭合K一段时间后,Ⅱ可单独作为原电池,d电极为正极 |
把物质的量均为0.1 mol的AlCl3、CuCl2和H2SO4溶于水配制成100 mL混合溶液,用石墨作电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下的体积相同。则下列描述正确的是( )
| A.电路中共转移0.9 mol电子 |
| B.阳极得到的气体中有O2,且其物质的量为0.35 mol |
| C.阴极的质量增加3.2 g |
| D.铝元素仅以Al(OH)3的形式存在 |
