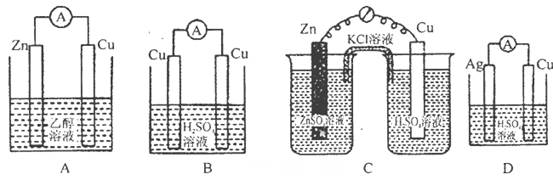
下列有关金属腐蚀与防护的说法正确的是
| A.纯银器表面在空气中会因化学腐蚀渐渐变暗 |
| B.地下输油钢管与外加直流电源的正极相连可保护其不受腐蚀 |
| C.海轮外壳连接锌块是采用牺牲阴极的阳极保护法保护外壳不受腐蚀 |
| D.当镀锡铁制品的镀层破损时,锡镀层仍能对铁制品起保护作用 |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH
溶液,其充、放电按下式进行:
有关该电池的说法正确的是( )。
A.充电时阳极反应: |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
如图所示a、b 都是惰性电极,通电—段时间后,a极附近溶液显红色。下列说法中正确的是( )。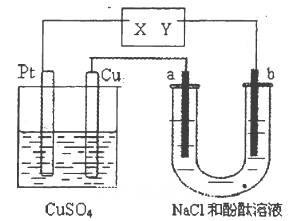
| A.X是正极,Y是负极 | B.X是负极,Y是正极 |
| C.CuSO4溶液的浓度逐渐减小 | D.CuSO4溶液的pH减小 |
某同学按图所示的装置进行电解实验,下列说法错误的是( )。
| A.电解初期,石墨电极上有H2产生 |
| B.整个电解过程中,H+的浓度不断增大 |
| C.电解一定时间后,石墨电极上有铜析出 |
D.电解初期,总反应方程式为: |
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入( )
| A.0.15 mol CuO | B.0.1 mol CuCO3 |
| C.0.075mol Cu(OH)2 | D.0.05 mol Cu2(OH)2CO3 |
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂溶解在亚硫酰氯(SOCl2)中形成,电池的总反应式为8Li+3SOCl2=6LiCl+Li2SO3+2S,则下列叙述正确的是 ( )
| A.用该电池电解CuCl2溶液产生2.24LCl2时,有0.2mol电子转移 |
| B.金属锂作电池的负极,石墨作电池的正极,加入硫酸可提高电解质的导电性 |
| C.电池工作(放电)过程中,SOCl2被还原为Li2SO3 |
| D.电池工作过程中,负极消耗的锂与正极生成的硫质量之比为7:8 |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A.氢氧燃料电池的负极反应式:O2 + 2H2O+ 4e- = 4OH - |
| B.铅蓄电池充电时,标示“+”的接线柱连电源的正极,电极反应式为:PbSO4(S)-2e - + 2H2O(l)=PbO2(S) + 4H+(aq)+ SO42-(aq) |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e- = Cu2+ |
| D.钢铁发生电化学腐蚀的正极反应式:Fe-2e - = Fe2+ |
某课外活动小组用如图所示装置进行实验(电解液足量)。下列说法中错误的是( )
| A.图1中,若开始实验时开关K与a连接,则B极的电极反应式为Fe-3e-=Fe3+ |
| B.图1中,若开始实验时开关K与b连接,则一段时间后向电解液中通入适量HCl气体可恢复到电解前的浓度 |
| C.图2中,若开始实验时开关K与a连接,则电解液的溶质质量分数变小 |
| D.图2中,若开始实验时开关K与b连接,则A极减少的质量等于B极增加的质量 |
目前人们掌握了可充电锌—空气电池技术,使这种电池有了更广泛的用途。这种电池使用特殊技术吸附空气中的氧,以苛性钠溶液为电解质,电池放电时的总反应为2Zn+O2=2ZnO,下列判断正确的是( )
| A.放电时,OH-向负极方向移动 |
| B.放电时,正极反应式为Zn+2OH--2e-=ZnO+H2O |
| C.充电时,Zn发生氧化反应 |
| D.充电时,阴极反应为O2+2H2O+4e-=4OH- |