镍氢电池的化学方程式为NiO(OH)+MH Nio+M+H2O(M为储氢合金,电解质
Nio+M+H2O(M为储氢合金,电解质
为KOH),下列说法不正确的是
| A.充电过程中,电池的负极上发生的反应为H2O +M+ e- =MH+OH- |
| B.储氢合金位于电池的负极 |
| C.放电时,OH-离子向电池的负极移动 |
| D.充电过程中,化学能转化为电能储存在电池中 |
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3—)=6.0 mol·L-1,用石墨做电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
| A.原混合溶液中c(K+)为2 mol·L-1 |
| B.上述电解过程中共转移6 mol电子 |
| C.电解得到的Cu的物质的量为0.5 mol |
| D.电解后溶液中c(H+)为2 mol·L-1 |
某化学学习小组学习电化学后,设计了下面的实验装置图: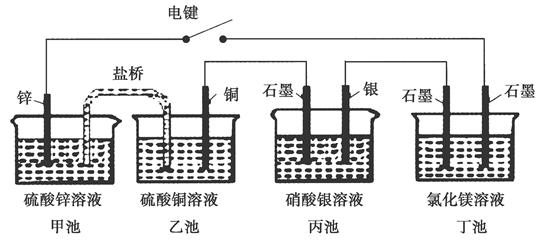
下列有关该装置图的说法中正确的是( )
| A.合上电键后,盐桥中的阳离子向甲池移动 |
| B.合上电键后,丙池为电镀银的电镀池 |
| C.合上电键后一段时间,丙池中溶液的pH增大 |
| D.合上电键后一段时间,当丙池中生成标准状况下560 mL气体时,丁池中理论上最多产生2.9 g固体 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
| A.充电时阳极反应为Zn-2e-+2OH-=Zn(OH)2 |
| B.充电时OH-向阳极移动 |
| C.放电时每转移3 mol e-正极有1 mol K2FeO4被氧化 |
| D.充电时,电源的正极应与电池的Zn(OH)2极相连 |
电化学在日常生活中用途广泛,图甲是镁—次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是( )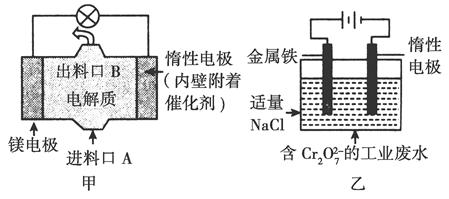
| A.图乙中Cr2O72-向惰性电极移动,与该极近的OH-结合转化成Cr(OH)3除去 |
| B.图乙的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生 |
| C.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓ |
| D.若图甲中3.6 g镁溶液产生的电量用以图乙废水处理,理论可产生10.7 g氢氧化铁沉淀 |
甲烷燃料电池,分别选择H2SO4溶液和NaOH溶液做电解质溶液,下列有关说法正确的是( )
| A.总反应式都为CH4+2O2=CO2+2H2O |
| B.H2SO4和NaOH的物质的量都不变,但浓度都减小 |
| C.若用H2SO4溶液做电解质溶液,负极反应式为CH4-4e-+H2O=CO2+4H+ |
| D.若用NaOH溶液做电解质溶液,正极反应式为O2+2H2O+4e-=4OH- |
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳。其中一种镁电池的反应为xMg+Mo3S4 MgxMo3S4,下列说法错误的是( )
MgxMo3S4,下列说法错误的是( )
| A.放电时Mg2+向正极迁移 |
| B.放电时正极反应为Mo3S4+2xe-=Mo3S42x- |
| C.充电时Mo3S4发生氧化反应 |
| D.充电时阴极反应为Mg2++2e-=Mg |
铜锌原电池(如图)工作时,下列叙述正确的是( )
| A.正极反应为Zn-2e-=Zn2+ |
| B.电池反应为Zn+Cu2+=Zn2++Cu |
| C.在外电路中,电子从负极流向正极 |
| D.盐桥中的K+移向ZnSO4溶液 |
