高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下:
Ni(OH)2+M NiOOH+MH,下列叙述正确的是 ( )
NiOOH+MH,下列叙述正确的是 ( )
| A.放电时正极附近溶液的碱性增强 |
| B.放电时负极反应为:M+H2O+e-=MH+OH- |
| C.充电时阳极反应为:NiOOH+H2O+e-=Ni(OH)2+OH- |
| D.放电时每转移1 mol电子,正极有1 mol NiOOH被氧化 |
实验发现,298 K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如图所示的原电池装置。下列有关说法中正确的是 ( )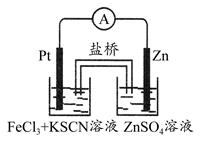
| A.该原电池的正极反应是:Zn-2e-=Zn2+ |
| B.左烧杯中溶液的红色逐渐褪去 |
| C.该电池铂电极上有气泡出现 |
| D.该电池总反应为:3Zn+2Fe3+=2Fe+3Zn2+ |
下列有关电化学知识的描述正确的是 ( )
| A.CaO+H2O=Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B.某原电池反应为Cu+2AgNO3=Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液 |
| C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 |
控制适合的条件,将反应Fe3++Ag Fe2++Ag+设计成如图所示的原电池。下列判断不正确的是 ( )
Fe2++Ag+设计成如图所示的原电池。下列判断不正确的是 ( )
| A.反应开始时,石墨棒作阳极,银棒作阴极 |
| B.灵敏电流计的读数由小变大,再变小 |
| C.反应达化学平衡时,电流计读数最小 |
| D.反应达化学平衡时,在乙烧杯中滴入一定量的NaCl溶液,电流计指针又将偏转 |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月。其电池反应为:2CH3OH+3O2+4OH- 2CO32—+6H2O,则下列说法正确的是( )
2CO32—+6H2O,则下列说法正确的是( )
| A.放电时CH3OH参与反应的电极为正极 |
| B.放电时负极的电极反应为CH3OH+8OH--6e-=CO32—+6H2O |
| C.标准状况下,通入5.6 L O2并完全反应后,有0.5 mol电子转移 |
| D.放电一段时间后,通入氧气的电极附近溶液的pH降低 |
下图是一种染料敏化太阳能电池的示意图。电池的一个电极由有机光敏染料(S)涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:
TiO2/S TiO2/S*(激发态)
TiO2/S*(激发态)
TiO2/S*―→TiO2/S++e-
I3—+2e-―→3I-
2TiO2/S++3I-―→2TiO2/S+I3—
下列关于该电池叙述错误的是 ( )
| A.电池工作时,I-在镀铂导电玻璃电极上放电 |
| B.电池工作时,是将太阳能转化为电能 |
| C.电池的电解质溶液中I-和I3—的浓度不会减少 |
| D.电池中镀铂导电玻璃为正极 |
电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一项重大贡献。下列有关电池的叙述正确的是 ( )
| A.锌锰干电池工作一段时间后碳棒变细 |
| B.氢氧燃料电池可将热能直接转变为电能 |
| C.氢氧燃料电池工作时氢气在负极被氧化 |
| D.太阳能电池的主要材料是高纯度的二氧化硅 |
据环保部门测定,我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极发生的反应是 ( )。
| A.Fe-2e-=Fe2+ |
| B.2H2O+O2+4e-=4OH- |
| C.2H++2e-=H2↑ |
| D.4OH--4e-=2H2O+O2↑ |
科学家从电解冶炼铝的工艺中得到启发,找出了冶炼钛的新工艺——TiO2直接电解法生产钛,电解质为熔融的氯化钙,原理如图所示。下列说法错误的是 ( )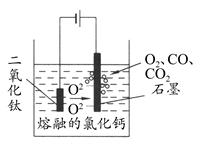
| A.阴极得到钛,电极反应式为TiO2+4e-=Ti+2O2- |
| B.阳极的电极反应式是2O2--4e-=O2↑,生成的部分氧气会将石墨氧化成CO和CO2 |
| C.在工业生产过程中应该不断地更换两极材料 |
| D.该法生产Ti符合绿色环保的要求 |
如图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑点向d端扩散。下列判断正确的是( )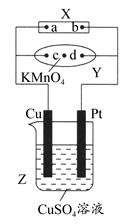
| A.滤纸上c点附近会变红色 |
| B.Cu电极质量减小,Pt电极质量增大 |
| C.Z中溶液的pH先减小,后增大 |
| D.溶液中的SO42—向Cu电极定向移动 |