某一元有机酸HA的溶液中,若未电离的HA分子个数与溶液中的离子个数比为a:b,则HA的电离度(即转化率)是
A. ×100% ×100% | B.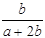 ×100% ×100% |
C.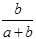 ×100% ×100% | D. ×100% ×100% |
在足量锌与等物质的量浓度、等体积的盐酸和醋酸反应时,下列叙述正确的是
| A.开始反应时,二者的速率相等 | B.盐酸放出的H2多 |
| C.二者放出的H2一样多 | D.醋酸消耗的Zn的质量多 |
在RNH2·H2O RNH3++OH-的平衡中,要使RNH2·H2O的电离程度及c(OH-)都增大,可采取的措施是
RNH3++OH-的平衡中,要使RNH2·H2O的电离程度及c(OH-)都增大,可采取的措施是
| A.通入HCl | B.加少量NaOH固体 | C.加水 | D.升温 |
在醋酸的电离过程中,加入水会使下列比值增大的是
| A.c(CH3COOH)/c(CH3COO—) | B.c(CH3COO—)/c(OH—) |
| C.c(H+)/c(CH3COOH) | D.c(H+)/ c(OH—) |
能说明醋酸是弱电解质的事实是
| A.醋酸水溶液能使湿润的蓝色石蕊试纸变红 |
| B.醋酸和碳酸钠溶液反应放出二氧化碳 |
| C.c(H+)相同的醋酸和盐酸相比较,醋酸溶液的浓度大 |
| D.物质的量浓度和体积均相同的醋酸和盐酸可中和等物质的量的NaOH |
下列有关叙述正确的是 ( )
| A.氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) |
| B.pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) |
C.室温下向10 mL pH=3的醋酸溶液中加水稀释,溶液中 不变 不变 |
| D.在0.1 mol·L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
在0.1mol/L的醋酸溶液中,存在平衡:CH3COOH CH3COO- +H+下列说法正确的是( )
CH3COO- +H+下列说法正确的是( )
| A.加水稀释,中和此溶液所需的0.1mol/LNaOH溶液的体积增大 |
| B.加入固体碳酸钠,平衡正向移动,c(CH3COOH)减小 |
| C.加入固体醋酸钠,平衡逆向移动,c(H+)、c(CH3COO-)均减小 |
| D.加水稀释,电离程度增大,由CH3COOH电离出来的n(H+)增大 |
25℃时,将稀氨水逐滴滴加到稀硫酸中,当溶液的pH=7时,下列关系正确的是( )
| A.c(NH4+)=c(SO42-) |
| B.c(NH4+)>c(SO42-) |
| C.c(NH4+)<c(SO42-) |
| D.c(NH4+)+c(SO42-)=c(H+)=c(NH4+) |
常温下,向10 mL 0.1 mol·L-1的H2C2O4溶液中逐滴加入0.1 mol·L-1 KOH溶液,所得滴定曲线如图所示。下列说法正确的是( )
| A.KHC2O4溶液呈弱碱性 |
| B.B点时:c(K+)>c(HC2O4-)>c(H+)>c(OH-) |
| C.C点时:c(HC2O4-)+c(C2O42-)+c(H2C2O4)<c(K+)<c(HC2O4-)+2c(C2O42-)+c(H2C2O4) |
| D.D点时:c(H+)+c(HC2O4-)+c(H2C2O4)=c(OH-) |
0.1mol·L-1Na2S溶液,下列关系正确的是
| A.c(Na+)=2c(S2-) |
| B.c(OH-)="c" (H+)+c (HS-)+2c (H2S) |
| C.c(Na+) >c(S2-) >c (HS-) >c (OH-) |
| D.c(Na+)+c (H+)="2c" (S2-)+c (HS-)+c (OH-) |