甲酸(HCOOH)的下列性质中,可以证明它是弱电解质的是
| A.甲酸溶液中有大量的HCOOH分子和H+、HCOO— |
| B.甲酸能与水以任意比例互溶 |
| C.10mL 1 mol/L甲酸恰好与10mL 1 mol/LNaOH溶液完全反应 |
| D.在相同温度下,相同浓度的甲酸溶液的导电性比盐酸弱 |
在某温度时,测得纯水中的c(H+)=2.4×10-7mol/L,则c(OH-)为
| A.2.4×10-7mol/L | B.0.1×10-7mol/L |
C.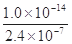 mol/L mol/L | D.无法确定 |
在25 ℃时,用蒸馏水稀释1 mol·L-1氨水至0.01 mol·L-1,随溶液的稀释,下列各项中始终保持增大趋势的是( )
| A.c(NH4+)/c(OH-) | B.c(OH-)/c(NH3·H2O) |
| C.c(NH3·H2O)/c(NH4+) | D.OH-物质的量 |
下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
| A.相同浓度的两溶液中c(H+)相同 |
| B.100mL0.1mol/L的两溶液能中和等物质的量的氢氧化钠 |
| C.pH=3的两溶液都稀释10倍,盐酸的pH大于醋酸的PH |
| D.两溶液中分别加人少量对应的钠盐,c(H+)均明显减小 |
下列关于强、弱电解质的叙述,有错误的是( )
| A.强电解质在溶液中完全电离,不存在电离平衡 |
| B.在溶液中,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 |
| C.强电解质都是离子化合物,弱电解质都是共价化合物 |
| D.纯净的强电解质在液态时,有的导电,有的不导电 |
下列有关“电离平衡”的叙述正确的是( )
| A.电解质在溶液里达到电离平衡时,分子的浓度和离子的浓度相等 |
| B.电离平衡时,由于分子和离子的浓度不断发生变化,所以说电离平衡是静态平衡 |
| C.电离平衡是相对的、暂时的外界条件改变时,平衡就会发生移动 |
| D.电解质达到电离平衡后,各种离子的浓度相等 |
可以判定某酸HA是弱电解质的事实是
| A.HA能与水以任意比互溶 |
| B.0.1 mol·L-1HA溶液的pH约为3 |
| C.HA可与NaHCO3反应放出CO2 |
| D.HA溶液的导电能力很差 |
在0.1 mol·L-1的CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+。对于该平衡,下列叙述正确的是
CH3COO-+H+。对于该平衡,下列叙述正确的是
| A.加水,反应速率增大,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.滴加少量0.1 mol·L-1HCl溶液,溶液中c(H+)减少 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
下列液体均处于25℃,有关叙述正确的是
| A.某物质的溶液pH<7,向该溶液中加入氢氧化钠溶液,Kw增大 |
| B.pH=8的NaOH溶液稀释100倍,其pH=6 |
| C.将1L 0.1mol·L-1的Ba(OH)2溶液稀释为2L,pH=12 |
| D.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |



