已知H2S能定量完成下列反应:R- +H2S(少量) HR + HS-, 2Z-+ H2S(少量)
HR + HS-, 2Z-+ H2S(少量) 2HZ + S2-。下列叙述正确的是
2HZ + S2-。下列叙述正确的是
| A.相同温度下电离平衡常数:Ki1(H2S)>Ki(HZ)>Ki2(H2S)>Ki(HR) |
| B.结合H+的能力:Z->S 2->R->HS- |
| C.同温同浓度下,溶液的pH值:NaHS>NaR>Na2S>NaZ |
D.HZ与Na2S反应的离子方程式:HZ +S2- HS- + Z- HS- + Z- |
常温下,pH=11的氨水和pH=1的盐酸等体积混合(混合溶液体积为两溶液体积之和),恰好完全反应,则下列说法错误的是
| A.氨水的浓度大于盐酸的浓度 |
| B.原氨水中有1%的含氮微粒为NH4+ |
| C.氨水中水电离出的c(H+)是盐酸中水电离出的c(H+)的100倍 |
| D.混合溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=5×10-4mol/L |
已知25℃时,0.l mol/L的碳酸氢钠溶液的pH为8.4,则关于该溶液的叙述错误的是
| A.滴加甲基橙溶液呈黄色 | B.c(HCO3-)>c(H2CO3)>c(CO32-) |
| C.c(OH-)=c(H+)+c( H2CO3)-c (CO32-) | D.加水稀释,c( H2CO3)/c(HCO3-)的比值减小 |
下列说法正确的是
A.向 溶液通入 溶液通入 ,可使水解平衡: ,可使水解平衡: 向正反应方向移动,则溶液pH增大 向正反应方向移动,则溶液pH增大 |
B.室温时,0.1mol 某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4 某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4 |
C.25℃时,pH=13的1.0 L Ba  溶液中含有的 溶液中含有的 |
| D.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
常温下,pH=12的氢氧化钠溶液pH=4的醋酸溶液等体积混合后恰好中和,忽略混合后溶液体积的变化,下列说法中正确的是
| A.混合前的醋酸约1%发生电离 | B.混合后的溶液中 |
| C.氢氧化钠和醋酸和浓度不相等 | D.混合后的溶液呈中性 |
下列事实中不能证明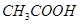 是弱电解质的是
是弱电解质的是
A.常温下某 |
B.常温下0.1mol 溶液的pH=2.8 溶液的pH=2.8 |
C. 溶液与稀盐酸反应生成 溶液与稀盐酸反应生成 |
D.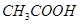 属于共价化合物 属于共价化合物 |
相同温度下,在水中分别加入下列物质,若用 表示水的离子积,a表示水的电离度,能使
表示水的离子积,a表示水的电离度,能使 的值增大的是
的值增大的是
| A.NaOH | B. | C.HC1 | D. |
已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列
有关说法正确的是( )
| A.除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
| B.向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强 |
| C.因为H2SO4是强酸,所以反应:CuSO4十H2S=CuS↓+H2SO4不能发生 |
| D.将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35mol/L |

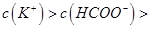

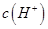

 ,且a=7.5
,且a=7.5

