已知草酸是二元弱酸,0.2 mol·L-1NaHC2O4溶液显酸性,关于NaHC2O4溶液中离子浓度关系的叙述不正确的是( )
| A.c(Na+)>c(HC2O4—)>c(C2O42—)>c(H2C2O4) |
| B.c(Na+)=c(HC2O4—)+c(C2O42—)+c(H2C2O4) |
| C.c(Na+)+c(H+)=c(HC2O4—)+c(C2O42—)+c(OH-) |
| D.c(H+)+c(H2C2O4)=c(C2O42—)+c(OH-) |
已知25℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100 mL该条件下的CaSO4饱和溶液中加入400 mL 0.01 mol·L-1Na2SO4溶液,针对此过程的下列叙述正确的是( )
| A.溶液中析出CaSO4沉淀,最终溶液中c(SO42—)较原来的大 |
| B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42—)都变小 |
| C.溶液中析出CaSO4沉淀,溶液中c(Ca2+)、c(SO42—)都变小 |
| D.溶液中无沉淀析出,但最终溶液中c(SO42—)较原来的大 |
25℃时,某难溶性碱MOH在水中的沉淀溶解平衡曲线如图所示(单位:mol·L-1)。下列说法正确的是( )
| A.该碱在25℃时的Ksp为2×10-10 |
| B.a点的Ksp大于b点的Ksp |
| C.通过蒸发可使溶液由b点变为c点 |
| D.25℃时,要使c(M+)为0.1 mol·L-1的溶液形成沉淀,溶液的pH至少要升高到5 |
25 ℃时,在浓度均为0.01 mol·L-1的NaCN与HCN组成的混合溶液中,测得c(Na+)>c(CN-),则下列描述中不正确的是( )
| A.该溶液的pH<7 |
| B.CN-的水解程度大于HCN的电离程度 |
| C.c(CN-)+c(HCN)=0.02 mol·L-1 |
| D.c(CN-)+c(OH-)=0.01 mol·L-1+c(H+) |
现有0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是( )
①电离程度增大;②c(NH3·H2O)增大;③N 数目增多;④c(OH-)增大;⑤导电性增强;⑥
数目增多;④c(OH-)增大;⑤导电性增强;⑥ 增大
增大
| A.①②③ | B.①③⑤ | C.①③⑥ | D.②④⑥ |
下表是三种难溶金属硫化物的溶度积常数(25 ℃)。
| 化学式 | FeS | CuS | MnS |
| 溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
下列有关说法中正确的是( )
A.25 ℃时,CuS的溶解度大于MnS的溶解度
B.25 ℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol/L
C.因为H2SO4是强酸,所以反应CuSO4+H2S
 CuS↓+H2SO4不能发生
CuS↓+H2SO4不能发生D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂
有常温下物质的量浓度均为0.1 mol/L的①氨水②NH4Cl溶液③Na2CO3溶液 ④NaHCO3溶液,下列说法正确的是( )
| A.4种溶液pH的大小顺序:①>④>③>② |
B.等体积的①和②溶液混合后若pH>7:c(Cl-)>c(N ) ) |
| C.溶液①、③由水电离产生的c(OH-):①<③ |
D.溶液③、④等体积混合后,溶液中c(C )>c(HC )>c(HC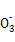 ) ) |
常温下,向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,正确的是( )
| A.HA可能为一元弱酸 |
| B.MOH为一元强碱 |
| C.N点水的电离程度小于K点水的电离程度 |
| D.若K点对应的溶液的pH=10,则有c(MOH)+c(M+)="0.01" mol·L-1 |
人体血液里存在重要的酸碱平衡: ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
| c(HCO3-):c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
下列说法不正确的是( )
A.正常人体血液中,HCO3-的水解程度大于电离程度
B.人体血液酸中毒时,可注射NaHCO3溶液缓解
C.pH=7.00的血液中,c(H2CO3)<c(HCO3-)
D.pH=7.40的血液中,HCO3-的水解程度一定大于H2CO3的电离程度
下列溶液中微粒浓度关系不正确的是( )
| A.常温下,氨水与氯化铵的pH=7的混合溶液中:c(Cl-)=c(NH4+) |
| B.pH=1的一元酸和pH=13的一元碱等体积混合:c(OH-)=c(H+) |
| C.0.1 mol·L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D.0.1 mol·L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S) |