壓T≧扮⇧蝶NaOH蓮卑匣嶄c(H⇦)﹆10⇩a mol,L⇩1⇧c(OH⇩)﹆10⇩b mol,L⇩1⇧厮岑a⇦b﹆12。﨑乎卑匣嶄幟砧紗秘pH﹆c議冦磨(T≧)⇧霞誼詞栽卑匣議何蛍pH泌和燕侭幣⦿
| 會催 | NaOH卑匣悶持 | 冦磨悶持 | 卑匣pH |
| 〙 | 20.00 | 0.00 | 8 |
| 〖 | 20.00 | 20.00 | 6 |
邪譜卑匣詞栽念朔議悶持延晒策待音柴⇧夸c葎↙ ⇄
A.1 B⤴4 C⤴5 D⤴6
25≧扮⇧壓吉悶持議〙pH﹆0議H2SO4卑匣、〖0.05 mol/L議Ba(OH)2卑匣、〗pH﹆10議Na2S卑匣、∠pH﹆5議NH4NO3卑匣嶄⇧窟伏窮宣議邦議麗嵎議楚岻曳頁↙ ⇄
| A⤴1|10|1010|109 | B⤴1|5|5〜109|5〜108 |
| C⤴1|20|1010|109 | D⤴1|10|104|109 |
和双偃峰屎鳩議頁↙ ⇄
| A⤴涙胎頁歓邦⇧珊頁磨來、珠來賜嶄來蓮卑匣⇧壓械梁和⇧凪c(H⇦),c(OH⇩)﹆1〜10⇩14 |
| B⤴c(H⇦)吉噐1〜10⇩7 mol/L議卑匣匯協頁嶄來卑匣 |
| C⤴0.2 mol/L CH3COOH卑匣嶄議c(H⇦)頁0.1 mol/L CH3COOH卑匣嶄議c(H⇦)議2蔚 |
| D⤴販採敵業議卑匣脅辛參喘pH栖燕幣凪磨珠來議膿樋。 |
壓0.1 mol,L⇩1CH3COOH卑匣嶄贋壓泌和窮宣峠財⦿CH3COOH CH3COO⇩⇦H⇦⇧斤噐乎峠財和双偃峰屎鳩議頁↙ ⇄
CH3COO⇩⇦H⇦⇧斤噐乎峠財和双偃峰屎鳩議頁↙ ⇄
| A⤴紗秘邦扮⇧峠財剃﨑卞強 |
| B⤴紗秘富楚NaOH耕悶⇧峠財屎﨑卞強 |
| C⤴紗秘富楚0.1 mol,L⇩1冦磨⇧卑匣嶄c(H⇦)受弌 |
| D⤴紗秘富楚CH3COONa耕悶⇧峠財屎﨑卞強 |
片梁和⇧喘0.100 mol/L NaOH 卑匣蛍艶砧協20.00 mL 0.100 mol/L議冦磨才閑磨⇧砧協爆㞍泌和夕侭幣。和双傍隈屎鳩議頁↙ ⇄
| A⤴↔、Å蛍艶燕幣冦磨才閑磨議砧協爆㞍 |
B⤴V(NaOH)﹆10.00 mL 扮⇧ ﹅1 ﹅1 |
| C⤴pH﹆7扮⇧曾嶽磨侭喘NaOH卑匣議悶持屢吉 |
| D⤴V(NaOH)﹆20 .00 mL 扮⇧c(Cl⇩)〽c(CH3COO⇩) |
壓t≧扮⇧AgBr壓邦嶄議柿牛卑盾峠財爆㞍泌夕侭幣。嗽岑t≧扮AgCl議Ksp﹆4〜10⇩10。和双傍隈音屎鳩議頁↙ ⇄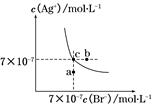
| A⤴壓t≧扮⇧AgBr議Ksp葎4.9〜10⇩13 |
| B⤴壓AgBr吋才卑匣嶄紗秘NaBr耕悶⇧辛聞卑匣喇c泣欺b泣 |
| C⤴夕嶄a泣斤哘議頁AgBr議音吋才卑匣 |
D⤴壓t≧扮⇧AgCl(s)⇦Br⇩(aq) AgBr(s)⇦Cl⇩(aq)峠財械方K「816 AgBr(s)⇦Cl⇩(aq)峠財械方K「816 |
片梁扮⇧M(OH)2(s) M2⇦(aq)⇦2OH⇩(aq) Ksp﹆a。c(M2⇦)﹆b mol,L⇩1扮⇧卑匣議pH吉噐↙ ⇄
M2⇦(aq)⇦2OH⇩(aq) Ksp﹆a。c(M2⇦)﹆b mol,L⇩1扮⇧卑匣議pH吉噐↙ ⇄
A⤴ lg( lg( ) ) | B⤴ lg( lg( ) ) |
C⤴14⇦ lg( lg( ) ) | D⤴14⇦ lg( lg( ) ) |
械梁和⇧函0.2 mol,L⇩1HX卑匣嚥0.2 mol,L⇩1 NaOH卑匣吉悶持詞栽(策待詞栽朔卑匣悶持議延晒)⇧霞誼詞栽卑匣議pH ﹆ 8⇧夸和双傍隈(賜購狼塀)屎鳩議頁↙ ⇄
| A⤴c(Na⇦)⇩c(X⇩)﹆9.9〜10⇩7mol,L⇩1 |
| B⤴c(Na⇦)﹆c(X⇩)⇦c(HX)﹆0.2 mol,L⇩1 |
| C⤴c(OH⇩)⇩c(HX)﹆c(H⇦)﹆1〜10⇩6mol,L⇩1 |
| D⤴詞栽卑匣嶄喇邦窮宣竃議c(OH⇩)﹆10⇩8mol,L⇩1 |
書嗤片梁和膨嶽卑匣,嗤購偃峰音屎鳩議頁( )
| | 〙 | 〖 | 〗 | ∠ |
| pH | 11 | 11 | 3 | 3 |
| 卑匣 | 葦邦 | 狽剳晒墜卑匣 | 閑磨 | 冦磨 |
A.〙、〖嶄蛍艶紗秘癖楚議柁晒錻唱悶朔,曾卑匣議pH譲受弌
B.蛍艶紗邦蓮瞥10蔚,膨嶽卑匣議pH:〙>〖>∠>〗
C.〙、∠曾卑匣吉悶持詞栽,侭誼卑匣嶄c(Cl-)>c(N
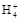 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)D.Va L ∠嚥Vb L 〖卑匣詞栽,飛詞栽朔卑匣pH=4,夸Va|Vb=11|9
械梁和,和双卑匣刃協格磨來議頁( )
| A⤴根H+議卑匣 | B⤴紗罫蜜𠮟涙弼議卑匣 |
| C⤴pH<7議卑匣 | D⤴c(OH-)>c(H+)議卑匣 |