25℃时,某浓度的氯化铵溶液的pH=4,下列叙述中不正确的是( )
| A.溶液中的c(OH-)=1×10-10 mol·L-1 |
| B.溶液中的c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C.溶液中的c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
| D.溶液中的c(NH3·H2O)=c(NH4+) |
下列叙述正确的是( )
| A.某醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a=b+1 |
| B.在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的c(NH4+) = c(Cl-) |
| C.25℃ 0.5×10-3 mol/L硫酸的pH=3.0,升高温度溶液pH增大 |
| D.100℃时,KW=10-12,若pH=1的盐酸与pH=11 NaOH溶液混合后,溶液的pH=6,则盐酸与NaOH溶液体积比为1∶1 |
水的电离平衡曲线如图所示,下列说法不正确的是 ( )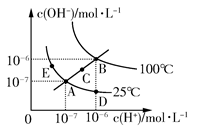
| A.图中五点KW间的关系:B>C>A=D=E |
| B.若从A点到D点,可采用在水中加入少量酸的方法 |
| C.若从A点到C点,可采用温度不变时在水中加入适量NH4Cl固体的方法 |
| D.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性 |
向含有H2SO4的CuSO4溶液中逐滴加入含a mol溶质的NaOH溶液,恰好使溶液的pH=7,下列叙述错误的是 ( )
| A.反应后溶液中c(Na+)=2c(SO42—) |
| B.a/2mol>沉淀的物质的量>0 |
| C.沉淀的质量=49a g |
| D.溶液中n(SO42—)=a/2 mol |
某温度下,CO2饱和溶液的浓度是0.03mol/L,其中1/3的CO2转变为H2CO3,而H2CO3仅有0.1%发生如下电离:H2CO3 H++HCO3—,则溶液的pH约为( )
H++HCO3—,则溶液的pH约为( )
| A.3 | B.4 | C.5 | D.6 |
已知相同条件下,HClO的电离常数小于H2CO3的一级电离常数(Ka)。为了提高氯水中HClO的浓度,可加入( )
| A.NaCl(s) | B.CaCO3(s) | C.H2O | D.NaOH(s) |
25℃时,水中存在电离平衡:H2O H++OH-。下列关于水的说法,不正确的是( )
H++OH-。下列关于水的说法,不正确的是( )
| A.水的电离是吸热过程 |
| B.向水中加入少量稀硫酸,c(H+)增大,KW不变 |
| C.含H+的溶液显酸性,含OH-的溶液显碱性 |
| D.水是极弱的电解质,在50℃时水的pH小于7 |
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见下图。下列说法正确的是 ( )
| A.在任何溶液中,c(Ca2+)、c(SO42—)均相等 |
| B.b点将有沉淀生成,平衡后溶液中c(SO42—)一定等于3×10-3mol·L-1 |
| C.a点对应的Ksp等于c点对应的Ksp |
| D.d点溶液通过蒸发可以变到c点 |
硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下,下列说法正确的是( )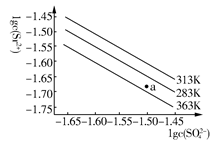
| A.温度一定时,Ksp(SrSO4)随c(SO42—)的增大而减小 |
| B.三个不同温度中,313 K时Ksp(SrSO4)最大 |
| C.283 K时,图中a点对应的溶液是饱和溶液 |
| D.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液 |