铝的以下反应得以进行的原因,可用勒沙特勒原理解释的是
| A.与盐酸反应产生氢气 |
| B.在氯气中燃烧 |
| C.放入硝酸汞溶液中表面形成铝汞齐 |
| D.一定温度下,用铝与氧化钙反应制得金属钙 |
一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应,在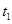 时达平衡:
时达平衡: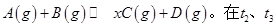 时刻分别改变反应的一个条件,测得溶器中C(g)的浓度随时间变化如图所示。有关说法正确的是
时刻分别改变反应的一个条件,测得溶器中C(g)的浓度随时间变化如图所示。有关说法正确的是
A.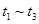 间该反应的平衡常数相同,均为0.25 间该反应的平衡常数相同,均为0.25 |
B.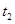 时刻改变的条件是使用催化剂 时刻改变的条件是使用催化剂 |
C. 时刻改变的条件是移去少量D 时刻改变的条件是移去少量D |
| D.反应方程式中x=2 |
下图表示反应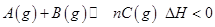 ,在不同条件下反应混合物中C的百分含量反应过程所需时间的关系曲线。下列有关叙述正确的是
,在不同条件下反应混合物中C的百分含量反应过程所需时间的关系曲线。下列有关叙述正确的是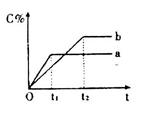
| A.反应由逆反应开始 |
| B.a表示有催化剂,b表示无催化剂 |
| C.若n=2,其它条件相同,a比b的压强大 |
| D.若其它条件相同,a比b的温度高 |
在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g)  2SO3(g) △H<0,n(SO2)随时间的变化如表:
2SO3(g) △H<0,n(SO2)随时间的变化如表:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 3 |
| n(SO2)/mol | 0.20 | 0.1 6 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是
A.当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B.用O2表示0~4min内该反应的平均速率为0.005mol/(L·min)
C.若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
D.平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
下列有关说法正确的是
| A.恒温时,向水中加入少量固体硫酸氢钠,c(H+)增大,水的离子积常数Kw不变 |
| B.0.1mol/LCH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
C.对于N2(g)+3H2(g) 2NH3(g),其他条件不变,充入N2,正反应速率增大,逆反应速率减小 2NH3(g),其他条件不变,充入N2,正反应速率增大,逆反应速率减小 |
| D.在硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
在一体积为10 L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g) CO2(g)+H2(g) △H<0。
CO2(g)+H2(g) △H<0。
(1)CO和H2O浓度变化如图,则在该温度下,该反应的平衡常数K= 。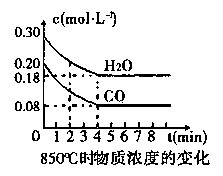
0~4 min的平均反应速率v(CO)= mol·L-1·min-1。若降低温度,该反应的K值将 ,该反应的化学反应速率将 (填“增大”“减小”或“不变”)。
(2)在相同容器中发生上述反应,当温度高于850℃时,容器内各物质的浓度变化如下表。
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 | |
①表中3 min~4 min之间反应处于 状态;cl数值 0.08 mol·L-1(填大于、小于或等于)。
②反应在4 min~5 min之间,平衡向逆方向移动,可能的原因是
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol·L-1,C(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是 。
取100 mL 2mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是
| A.加入适量的6mol/L的盐酸 | B.用酒精灯适当加热 |
| C.加入适量蒸馏水 | D.加入适量的氯化钠溶液 |
如下图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器。当其它条件相同时,在Ⅰ、Ⅱ中分别加入2 mol X和2 mol Y,开始时容器的体积均为V L,发生如下反应并达到平衡状态: 2X(?)+Y(?)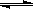 aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是( )
aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是( )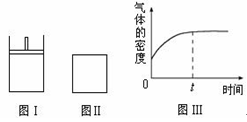
| A.物质Z的化学计量数a = 2 |
| B.若Ⅱ中气体的密度如图Ⅲ所示,则X、Y中只有一种为气态 |
| C.若X、Y均为气态,则在平衡时X的转化率:Ⅰ﹤Ⅱ |
| D.若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ |
在一定条件下,向一体积为2 L的恒容密闭容器中充入2 mol A,1 mol B,发生反应:2A(g)+B 3C(g) ΔH=-Q kJ/mol(Q>0)。经过60 s达到平衡,测得B的物质的量为0.2 mol,下列对该平衡的叙述正确的是( )
3C(g) ΔH=-Q kJ/mol(Q>0)。经过60 s达到平衡,测得B的物质的量为0.2 mol,下列对该平衡的叙述正确的是( )
| A.用C的浓度变化表示该反应速率为2.4 mol/(L·min) |
| B.若使容器变为1 L,则C的物质的量一定增大 |
| C.达到平衡,测得放出热量为x kJ,则x=Q |
| D.若向容器中再充入1 mol C,重新达到平衡,A的体积分数保持不变,则B为气态 |
已知可逆反应:M(g)+N(g) P(g)+Q(g) △H>0 。反应达到平衡后,若要增大M的转化率,在其它条件不变的情况下可以采取的措施为( )
P(g)+Q(g) △H>0 。反应达到平衡后,若要增大M的转化率,在其它条件不变的情况下可以采取的措施为( )
①加入一定量的M ②加入一定量的N ③升高反应体系的温度 ④缩小容器体积
⑤加入某物质作催化剂 ⑥分离出一定量的P
| A.①③⑤ | B.②④⑥ | C.②③⑥ | D.④⑤⑥ |