已知图一表示的是可逆反应CO(g)+H2(g) C(s)+H2O(g) ΔH>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)
C(s)+H2O(g) ΔH>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g) N2O4(g) ΔH<0的浓度(c)随时间(t)的变化情况。下列说法中正确的是( )
N2O4(g) ΔH<0的浓度(c)随时间(t)的变化情况。下列说法中正确的是( )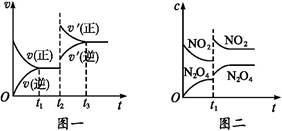
| A.图一t2时改变的条件可能是升高了温度或增大了压强 |
| B.图一t2时改变的条件一定是增大了反应物的浓度 |
| C.图二t1时改变的条件可能是升高了温度或增大了压强 |
| D.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小 |
下列叙述中能判断某化学平衡发生移动的是( )
| A.混合物中各组分的浓度改变 |
| B.正、逆反应速率改变 |
| C.混合物中各组分的含量改变 |
| D.混合体系的压强发生改变 |
下列条件一定能使反应速率加大的是( )
①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积 ④不断分离出生成物 ⑤加入MnO2
| A.①②③④⑤ | B.①②⑤ | C.② | D.②③ |
在5 mL 0.1 mol·L-1 KI溶液中滴加0.1 mol·L-1 FeCl3溶液5~6滴后,再进行下列实验,其中可证明FeCl3与KI的反应是可逆反应的实验(含现象)是( )
| A.滴加AgNO3溶液,有黄色沉淀产生 |
| B.加入CCl4振荡,下层液体为浅紫色 |
| C.加入CCl4振荡,下层液体为浅紫色;取上层清液,滴加AgNO3溶液,有白色沉淀产生 |
| D.加入CCl4振荡,下层液体为浅紫色;取上层清液,滴加KSCN溶液,溶液显红色 |
某温度下,反应X(g)+3Y(g) 2Z(g)的平衡常数为1 600。此温度下,在容积一定的密闭容器中加入一定量的X和Y,反应到某时刻测得各组分的浓度如下:
2Z(g)的平衡常数为1 600。此温度下,在容积一定的密闭容器中加入一定量的X和Y,反应到某时刻测得各组分的浓度如下:
下列说法正确的是( )
| A.此时v(正)<v(逆) |
| B.平衡时Y的浓度为0.05 mol·L-1 |
| C.平衡时X的转化率为40% |
| D.增大压强使平衡向正反应方向移动,平衡常数增大 |
在1 100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g) Fe(s)+CO2(g)ΔH="a" kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
Fe(s)+CO2(g)ΔH="a" kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A.若生成1 mol Fe,则吸收的热量小于a kJ |
| B.若要提高CO的转化率,则应该加入适当的过量FeO |
| C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D.达到化学平衡状态时,若c(CO)="0.100" mol/L,则c(CO2)="0.026" 3 mol/L |
设反应①Fe(s)+CO2(g) FeO(s)+CO(g) ΔH="a" kJ/mol,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH="a" kJ/mol,反应②Fe(s)+H2O(g) FeO(s)+H2(g) ΔH="b" kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH="b" kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下: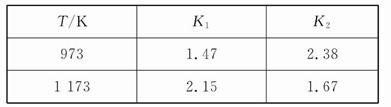
下列有关叙述正确的是( )
| A.b>0 | B.在973K下增大压强,K2增大 |
| C.a>b | D.在常温下反应①一定能自发进行 |
汽车尾气净化中的一个反应如下:2NO(g)+2CO(g) N2(g)+2CO2(g)ΔH=-746.8 kJ·mol-1,在恒容的密闭容器中,反应达到平衡后,当改变其中一个条件X,Y随X的变化,符合图中曲线的是( )
N2(g)+2CO2(g)ΔH=-746.8 kJ·mol-1,在恒容的密闭容器中,反应达到平衡后,当改变其中一个条件X,Y随X的变化,符合图中曲线的是( )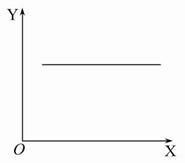
| A.当X表示温度时,Y表示平衡常数K |
| B.当X表示温度时,Y表示CO的转化率 |
| C.当X表示N2的物质的量时,Y表示NO的转化率 |
| D.当X表示NO的物质的量时,Y表示平衡常数K |
 CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法中正确的是( )
CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法中正确的是( )