已知:4NH3+5O2 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O) [mol/(L·min)]表示,则正确的关系式是( )
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O) [mol/(L·min)]表示,则正确的关系式是( )
A. v(NH3)=v(O2) v(NH3)=v(O2) | B.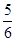 v(O2)=v(H2O) v(O2)=v(H2O) |
C.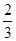 v(NH3)=v(H2O) v(NH3)=v(H2O) | D. v(O2)=v(NO) v(O2)=v(NO) |
一定条件下存在反应:2SO2(g)+O2 (g) 2SO3(g),其正反应放热。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
2SO3(g),其正反应放热。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
| A.容器I、Ⅲ中平衡常数相同 |
| B.容器II、Ⅲ中正反应速率相同 |
| C.容器Ⅱ、中的反应达平衡时,SO3的体积分数:II > III |
| D.容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1 |
下列有关说法正确的是
A.氨水稀释后,溶液中 的值减小 的值减小 |
| B.0.1 mol·L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 |
| C.电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 |
| D.298 K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其ΔH<0 |
已知甲为恒压容器、乙为恒容容器。。发生反应:2NO2(g) N2O4 (g) △H<0。一段时间后相继达到平衡状态。下列说法中正确的是( )
N2O4 (g) △H<0。一段时间后相继达到平衡状态。下列说法中正确的是( )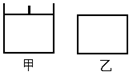
| A.平衡时NO2体积分数:甲<乙 |
| B.达到平衡所需时间,甲与乙相等 |
| C.该反应的平衡常数表达式K=c(N2O4)/c(NO2) |
| D.若两容器内气体的压强保持不变,均说明反应已达到平衡状态 |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是( )
A.反应的化学方程式为:X(g)+Y(g) Z(g) Z(g) |
| B.反应开始到10s时,Y的转化率为79.0% |
| C.反应开始到10s,X的物质的量浓度减少了 0.79mol/L |
| D.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s) |
某密闭容器中,可逆反应 L(s)+G(g) 3R(g) ΔH>0,如图表示外界条件温度、压强的变化对上述反应的影响。下列表述正确的是( )
3R(g) ΔH>0,如图表示外界条件温度、压强的变化对上述反应的影响。下列表述正确的是( )
| A.该反应达平衡后加入适当的催化剂可提高G的转化率 |
| B.达到平衡后向容器中加入L,平衡向右移动,G的转化率增大 |
| C.图中的y可能是平衡混合气中G的质量分数 |
| D.图中的y可能是达到平衡时G的转化率 |
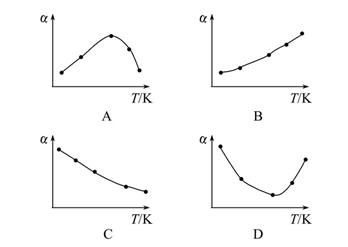
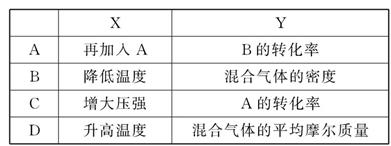
在某恒容的密闭容器中,可逆反应A(g)+B(g) xC(g)有如图所示的关系曲线,下列说法正确的是( )
xC(g)有如图所示的关系曲线,下列说法正确的是( )
| A.温度:T1>T2 | B.压强:p1>p2 |
| C.正反应是吸热反应 | D.x的值是2 |
在容积一定的密闭容器中,反应A(?)+B(g) C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是( )
C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是( )
| A.正反应是放热反应 |
| B.A不是气态物质,加入A该平衡向正反应方向移动 |
| C.其他条件不变,加入A平衡不移动 |
| D.改变压强对该平衡的移动无影响 |