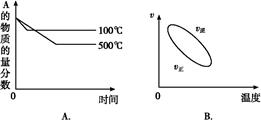
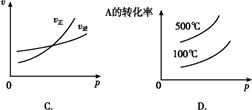
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)  2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
| 压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1 000 | e | f | 83.0 |
① b<f ② 915℃、2.0 MPa时E的转化率为60%③ 增大压强平衡左移 ④ K(1 000℃)>K(810℃)
上述①~④中正确的有( )
A.4个 B.3个 C.2个 D.1个
在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g)  2c(g) ΔH1<0
2c(g) ΔH1<0
x(g)+3y(g)  2z(g) ΔH2>0
2z(g) ΔH2>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( )
| A.等压时,通入惰性气体,c的物质的量不变 |
| B.等压时,通入z气体,反应器中温度升高 |
| C.等容时,通入惰性气体,各反应速率不变 |
| D.等容时,通入z气体,y的物质的量浓度增大 |
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g)??2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )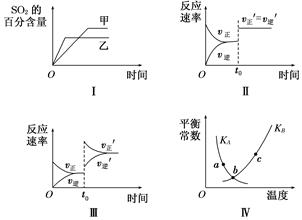
| A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响 |
| C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |
| D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |
在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中发生下述反应:PCl3(g)+Cl2(g) PCl5(g),5 min末达到平衡,有关数据如表。
PCl5(g),5 min末达到平衡,有关数据如表。
| | PCl3(g) | Cl2(g) | PCl5(g) |
| 初始浓度(mol·L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol·L-1) | c1 | c2 | 0.4 |
下列判断不正确的是( )
A.若升高温度,反应的平衡常数减小,则正反应为吸热
B.反应5 min内,v(PCl3)="0.08" mol·L-1·min-1
C.当容器中Cl2为1.2 mol时,可逆反应达到平衡状态
D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol·L-1
在容积一定的密闭容器中发生可逆反应A(g)+2B(g) 2C(g) ΔH>0;平衡移动关系如图所示。下列说法正确的是( )
2C(g) ΔH>0;平衡移动关系如图所示。下列说法正确的是( )
| A.p1<p2,纵坐标指A的质量分数 |
| B.p1>p2,纵坐标指C的质量分数 |
| C.p1<p2,纵坐标指A的转化率 |
| D.p1<p2,纵坐标指混合气体的平均摩尔质量 |
利用反应:2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH ="+746.8" kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是 ( )
2CO2(g)+N2(g) ΔH ="+746.8" kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是 ( )
| A.降低温度 |
| B.增大压强同时加催化剂 |
| C.升高温度同时充入N2 |
| D.及时将CO2和N2从反应体系中移走 |
在恒温下的密闭容器中,有可逆反应:2NO2 N2O4,下列不能说明反应达到了平衡状态的是 ( )
N2O4,下列不能说明反应达到了平衡状态的是 ( )
| A.N2O4生成速率与N2O4分解速率相等时 |
| B.混合气体平均相对分子质量保持不变时 |
| C.NO2的分子数与N2O4分子数比为2∶1时 |
| D.体系颜色不再发生改变时 |