等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得到右上图,则曲线a、b、c、d所对应的实验组别可能是( )
| 组别 | c(HCl)(mol·L-1) | 温度(℃) | 状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.5 | 50 | 块状 |
| 4 | 2.5 | 30 | 粉末状 |
A.4、3、2、1 B.1、2、3、4
C.3、4、2、1 D.1、2、4、3
其他条件不变时,能使反应速率加快的是( )
| A.对于反应Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,增大体系的压强 |
B.对于N2(g)+3H2(g) 2NH3(g),容器体积固定不变时,充入Ar 2NH3(g),容器体积固定不变时,充入Ar |
C.对于N2(g)+3H2(g) 2NH3(g),容器体积固定不变时,充入N2 2NH3(g),容器体积固定不变时,充入N2 |
D.对于N2(g)+3H2(g) 2NH3(g),容器气体压强不变时,充入Ar 2NH3(g),容器气体压强不变时,充入Ar |
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应反应过程中H2、N2和NH3物质的量变化如下图所示,下列说法正确的是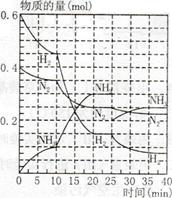
| A.反应开始到第一次平衡时,N2的平均反应速率为0.005 mol/(L·min) |
| B.从曲线可以看出,反应进行到10min至20min时可能是使用了催化剂 |
| C.从曲线可以看出,反应进行至25min时,增加了0.1mol氨气 |
| D.在25min平衡正向移动但达到新平衡后NH3的体积分数比原平衡小 |
在一个6L的密闭容器中放入3mol X和2molY,在一定条件下发生反应4X(g)+3Y(g) 2Q(g)+nR(g),达到平衡后,容器内的压强比原来增加5%,X浓度减小
2Q(g)+nR(g),达到平衡后,容器内的压强比原来增加5%,X浓度减小 ,则该反应方程式中的n值是( )
,则该反应方程式中的n值是( )
| A.3 | B.4 | C.5 | D.6 |
对于2SO2+O2 2SO3的反应,下列叙述中正确的是( )
2SO3的反应,下列叙述中正确的是( )
| A.“高温”和“催化剂”的条件使SO2和O2产生了可发生性 |
| B.“高温”和“催化剂”的条件可加快SO3分解为SO2和O2 |
| C.在该反应的平衡状态,SO2、SO2、O2的浓度一定都相等 |
| D.在该反应的平衡状态,正反应速率和逆反应速率相等 |
下列关于物质“反应程度”的说法正确的是( )
| A.一定条件下,2molsO2与足量O2反应可得到2molsO3 |
| B.含4mol HCl的浓盐酸与足量的MnO2加热反应可制备1mol Cl2 |
| C.10mL 18.0mol/L H2SO4与足量铜加热反应可制备0.09molsO2 |
| D.一定条件下,1mol N2与3mol H2反应可制备1.0mol NH3 |
一定条件下,可逆反应2A(g) B(g)+3C(g),下列四项中处于平衡状态的是( )
B(g)+3C(g),下列四项中处于平衡状态的是( )
| | 正反应速率 | 逆反应速率 |
| A | v(A)=2mol/(L·min) | v(B)=2mol/(L·min) |
| B | v(A)=2mol/(L·min) | v(C)=2mol/(L·min) |
| C | v(A)=1mol/(L·min) | v(B)=2mol/(L·min) |
| D | v(A)=1mol/(L·min) | v(C)=1.5mol/(L·min) |
 xC(g) △H<0。测得两容器中c(A)随时间t的变化如右图所示,下列说法错误的是
xC(g) △H<0。测得两容器中c(A)随时间t的变化如右图所示,下列说法错误的是