在一定条件下,CO(g)和H2(g)发生反应:CO(g) + 2H2(g)  CH3OH(g) △H=akJ/mol在容积固定的2L密闭容器中充入2mol CO(g)和4molH2(g)发生反应,测定在不同温度、不同时段下CO的转化率如下表:
CH3OH(g) △H=akJ/mol在容积固定的2L密闭容器中充入2mol CO(g)和4molH2(g)发生反应,测定在不同温度、不同时段下CO的转化率如下表: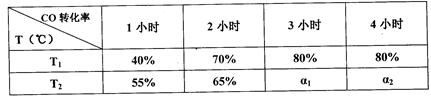
下列说法中正确的是
| A.热化学方程式中a>0 |
| B.T1℃下,在第一小时内用H2表示的化学反应速率为0.4mol/(L.h) |
| C.T1℃下,该反应的化学平衡常数为25 |
| D.T2℃下,ɑ1=ɑ2﹥80% |
在一容积可变的密闭容器中进行反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),下列有关叙述不正确的是
Fe3O4(s)+4H2(g),下列有关叙述不正确的是
| A.增加Fe的量,正反应速率不变 |
| B.将容器的体积缩小一半,正逆反应速率增大 |
| C.保持体积不变,充入Ne,正逆反应速率增大 |
| D.保持压强不变,充入Ne,正逆反应速率变小 |
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:
2X(g)+Y(g) Z(g)△H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是( )
Z(g)△H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是( )
| A.以Y浓度变化表示的反应速率为0.0005 mol/(L·s) |
| B.其他条件不变,将容器体积扩大至20 L,则Z的平衡浓度变为原来的1/2 |
| C.其他条件不变,将容器体积缩小至5L,平衡正向移动,平衡常数增大 |
| D.其他条件不变,升高温度逆反应速率加快,正反应速率减慢 |
在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g)+Y(g) 3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
| A.升高温度,平衡常数增大 |
| B.W点X的正反应速率等于M点X的正反应速率 |
| C.Q点时,Y的转化率最大 |
| D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
1 mol X气体跟a mol Y气体在体积可变的密闭容器中发生如下反应:
X(g)+aY(g) bZ(g)
bZ(g)
反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是( )
| A.a=1,b=1 | B.a=2,b=1 |
| C.a=2,b=2 | D.a=3,b=3 |
放热反应CO(g)+H2O(g) CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol·L-1,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则 ( )
CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol·L-1,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则 ( )
| A.K2和K1的单位均为 mol·L-1 |
| B.K2>K1 |
| C.c2(CO)=c2(H2O) |
| D.c1(CO)>c2(CO) |
250°C和1.01×105Pa时,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=+56.76 kJ/mol,自发进行的原因是( )
| A.是吸热反应 | B.是放热反应 | C.是熵减反应 | D.熵增效应大于能量效应 |
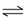 C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )

 cC(g);5min时,测得C为xmol。下列说法中一定正确的是( )
cC(g);5min时,测得C为xmol。下列说法中一定正确的是( )