高温下,某反应达平衡,平衡常数K=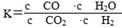 ,恒容时,温度升高,H2浓度减小。下列说法正确的是( )
,恒容时,温度升高,H2浓度减小。下列说法正确的是( )
| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为CO+H2O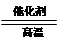 CO2+H2 CO2+H2 |
[双选题]可逆反应2A(g)+B(g) 3C(?)+D(?) ΔH<0,其他条件不变,随着温度的降低,混合气体平均相对分子质量有变小的趋势,则下列判断正确的是( )
3C(?)+D(?) ΔH<0,其他条件不变,随着温度的降低,混合气体平均相对分子质量有变小的趋势,则下列判断正确的是( )
| A.C和D可能都是固体 |
| B.C和D一定都是气体 |
| C.若D为固体,则C一定是气体 |
| D.C和D可能都是气体 |
已知:A(s)+B(g) 2D(g) ΔH>0,该反应达到平衡后,下列条件的改变有利于平衡向正反应方向移动的是( )
2D(g) ΔH>0,该反应达到平衡后,下列条件的改变有利于平衡向正反应方向移动的是( )
| A.升高温度和减小压强 | B.降低温度和减小压强 |
| C.降低温度和增大压强 | D.升高温度和增大压强 |
25℃和1.01×105 Pa时,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=56.76 kJ·mol-1能自发进行的原因是( )
| A.是吸热反应 | B.是放热反应 |
| C.是熵减少的反应 | D.熵增大效应大于能量效应 |
相同温度下,体积均为1.5 L的两个恒容容器中发生可逆反应:
X2 (g+3Y2(g)  2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热46.3 kJ |
| ② | 0.8 | 2.4 | 0.4 | Q(Q>0) |
下列叙述不正确的是
A.容器①中达到平衡时,Y2的转化率为50%
B.Q="27.78" kJ
C.若容器①体积改为1.0 L.则达平衡时放出的热量大于46.3 kJ
D.容器①、②中反应的平衡常数相等,K=
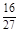
恒温下,反应aX(g)  bY(g)+cZ(g)达到平衡状态,把容器体积压缩到原来的1/2,且达到新的平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L,下列判断正确的是( )
bY(g)+cZ(g)达到平衡状态,把容器体积压缩到原来的1/2,且达到新的平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L,下列判断正确的是( )
| A.a>b+c | B.a<b+c |
| C.a=b+c | D.a=b=c |
下列说法不正确的是( )
| A.焓变是一个反应能否自发进行相关的因素,多数放热反应能自发进行 |
| B.自发进行的反应一定能迅速进行 |
| C.在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大 |
| D.一个反应能否自发进行,可用焓变和熵变共同判断 |
在某密闭容器中,可逆反应:A(g)+B(g) xC(g)符合图像(Ⅰ)所示关系。由此推断,对图像(Ⅱ)的不正确的说法是( )
xC(g)符合图像(Ⅰ)所示关系。由此推断,对图像(Ⅱ)的不正确的说法是( )
| A.p3>p4,y轴表示A的转化率 |
| B.p3>p4,y轴表示B的质量分数 |
| C.p3>p4,y轴表示C的质量分数 |
| D.p3>p4,y轴表示混合气体的平均相对分子质量 |

