已知充分燃烧a g乙炔(C2H2)气体时生成1 mol CO2气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
| A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-4b kJ·mol-1 |
B.C2H2(g)+ O2(g)=2CO2(g)+H2O(l)ΔH=2b kJ·mol-1 O2(g)=2CO2(g)+H2O(l)ΔH=2b kJ·mol-1 |
| C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-2b kJ·mol-1 |
| D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-b kJ·mol-1 |
下列说法正确的是
| A.吸热反应在常温下一定不能发生 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.已知C(石墨,s)=C(金刚石,s),△H1>0,说明石墨比金刚石稳定 |
D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的 不同 不同 |
已知:C(s,石墨) ="=" C(s,金刚石) ΔH =" +1.9" kJ·mol-1。下列有关说法正确的是
| A.相同条件下,1 mol石墨比1 mol金刚石能量高 |
| B.断裂1mol石墨中的化学键吸收的能量比断裂1mol金刚石中的化学键吸收的能量少 |
| C.若:C(s,石墨) + O2(g)==CO2(g) ΔH1=-393.5 kJ?mol-1 则有:C(s,金刚石) + O2(g)==CO2(g)ΔH2=-395.4 kJ·mol-1 |
| D.其他条件不变时,加入合适的催化剂,可实现该反应的反应热转变为ΔH<0 |
碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
① H2(g)+I2(?) 2HI(g)+9.48kJ② H2(g)+I2(?)
2HI(g)+9.48kJ② H2(g)+I2(?) 2HI(g)-26.48kJ
2HI(g)-26.48kJ
下列判断正确的是
| A.①中的I2为固态,②中的I2为气态 |
| B.②的反应物总能量比①的反应物总能量低 |
| C.①的产物比反应②的产物热稳定性更好 |
| D.1mol 固态碘升华时将吸热17kJ |
甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。
已知:CH3OH(l)+O2(g)= CO(g)+2H2O(g) 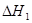 ="-443.64" kJ·mol-1
="-443.64" kJ·mol-1
2CO(g)+ O2(g)= 2CO2(g) 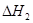 = -566.0kJ·mol-1
= -566.0kJ·mol-1
下列说法或热化学方程式正确的是
| A.CO的燃烧热为566.0 kJ·mol-1 |
| B.2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低 |
| C.完全燃烧20g甲醇,生成二氧化碳和水蒸气时放出的热量为908.3 kJ |
D.2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g)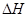 ="-1453.28" kJ·mol-1 ="-1453.28" kJ·mol-1 |
下列有关热化学方程式的叙述正确的是( )
| A.已知2H2(g)+O2(g)= 2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| B.已知C(石墨,s)= C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol |
| D.已知2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)=2CO(g) ;△H2。则△H1<△H2 |
下列变化过程,属于放热反应的是( )
①液态水变成水蒸气 ②酸碱中和反应 ③浓H2SO4稀释
④固体NaOH溶于水 ⑤H2在Cl2中燃烧 ⑥弱酸电离
| A.②③④⑤ | B.②③④ | C.②⑤ | D.①③⑤ |
拆开1 mol 共价键所吸收的能量或形成1 mol 共价键所释放的能量称为键能。已知:H-H键能为436 kJ /mol,H-N键能为391 kJ /mol, N2 (g)+ 3H2(g) 2NH3(g) ΔH=-92.4 kJ /mol,下列说法中正确的是
2NH3(g) ΔH=-92.4 kJ /mol,下列说法中正确的是
| A.H-H比N≡N更牢固 |
| B.N≡N键能约为946 kJ/mol |
| C.合成氨反应选择适当的催化剂是为了提高H2的转化率 |
| D.0.5 mol N2和1.5 mol H2在题给条件下充分反应,放出热量为46.2 kJ |
下列热化学方程式书写正确的是(△H的绝对值均为正确值)
| A.2NO2=O2+2NO△H=+116.2 kJ/mol(反应热) |
| B.S(s)+O2(g)=SO2(g)△H=-296.8 kJ/mol(反应热) |
| C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3 kJ/mol(中和热) |
| D.C2H5OH(l)+2O2(g)=2CO (g)+3H2O(g)△H=-801 kJ/mol(燃烧热) |