关于中和热测定实验的下列说法不正确的是
| A.烧杯间填满碎泡沫塑料是为了减少实验过程中的热量损失 |
| B.使用环形玻璃棒既可以搅拌又避免损坏温度计 |
| C.向盛装酸的烧杯中加碱时要小心缓慢 |
| D.测了酸后的温度计要用水清洗后再测碱的温度 |
下列说法中,错误的是
| A.人类目前所直接利用的能量大部分是由化学反应产生的 |
| B.化学变化中的能量变化主要是由化学键变化引起的 |
| C.化学反应中能量变化的大小与反应物的质量多少无关 |
| D.能量变化是化学反应的基本特征之一 |
下列说法不正确的是( )
| A.煤转化为煤气后燃烧,可以提高燃烧效率 |
| B.在生产、流通和消费等过程中实行“减量化、再利用、资源化” |
| C.化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体 |
| D.天然气是气体,它不属于化石燃料 |
下列说法中,正确的是( )
| A.化学反应除了生成新物质外,还伴随着能量的变化 |
| B.放热反应不需要加热就可以发生 |
| C.反应条件为加热的反应都是吸热反应 |
| D.化学反应放热还是吸热,取决于反应条件 |
已知:H+(aq)+OH-(aq) =H2O(l); △H=-57.3 kJ·mol-1。现将一定量的稀盐酸、浓硫酸、稀醋酸分别和1L 1mol·L-1的NaOH溶液恰好完全反应,其反应热分别为△H1、△H2、△H3,,则△H1、△H2和△H3的大小关系为
| A.△H1=△H2 | B.△H2>△H1 |
| C.△H3>△H2 | D.△H1>△H3 |
能够表示燃烧热的是( )
| A.2H2(g)+O2(g)=2H2O(g);△H1 |
| B.S(g)+O2(g)= SO2 (g);△H1 |
C.C(s)+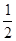 O2(g)= CO(g);△H1 O2(g)= CO(g);△H1 |
| D.H2(g)+Cl2(g) = 2HCl(g);△H1 |
相同温度下,甲(恒容)、乙(恒压)、丙(恒容)3个密闭容器中发生可逆反应:
2SO2(g)+O2(g) 2SO3(g)ΔH =" -197" kJ/mol。实验测得起始、平衡时的有关数
2SO3(g)ΔH =" -197" kJ/mol。实验测得起始、平衡时的有关数
据如下表。下列正确的是
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | ||
| SO2 | O2 | Ar | ||
| 甲 | 2 | 1 | 0 | 放出热量:Q1 |
| 乙 | 2 | 1 | 0 | 放出热量:Q2 |
| 丙 | 2 | 1 | 0.5 | 放出热量:Q3 |
A.Q1 =Q3<Q2
B.达到平衡时,乙容器中SO2的体积分数最大
C.平衡时,甲、乙、丙3个容器中甲的平衡常数最小
D.若在上述条件下,反应生成1molSO3(s),则反应放热为98.5kJ
下列有关热化学方程式的叙述正确的是
| A.已知2H2O(g) =2H2(g)+O2(g) △H=+483.6 kJ/mol,则氢气的燃烧热为△H=-241.8kJ/mol |
| B.已知C(石墨,s)= C(金刚石,s)△H>0,则金刚石不如石墨稳定 |
| C.已知中和热为△H=-57.4kJ/mol,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) △H=-57.4kJ/mol |
| D.已知2C(s)+2O2(g)=2CO2 (g) △H1;2C(s)+O2 (g)=2CO(g) △H2,则△H1>△H2 |
已知:P4(g)+6Cl2(g)=4PCl3(g) △H=a kJ?mol—1、P4(g)+10Cl2(g)=4PCl5(g) △H=b kJ?mol—1
P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ?mol—1,PCl3中P-Cl键的键能为1.2c kJ?mol—1。下列叙述正确的是
| A.P-P键的键能大于P-Cl键的键能 |
| B.可求Cl2(g)+ PCl3(g)=4PCl5(s)的反应热△H |
| C.Cl-Cl键的键能为(b-a+5.6c)/4 kJ?mol—1 |
| D.P-P键的键能为(5a-3b+12c)/8 kJ?mol—1 |
