在一定条件下,将64 g二氧化硫气体氧化成三氧化硫气体时,实验测得放出热量为78.64 kJ,已知二氧化硫在此条件下的转化率为80%。下列热化学方程式书写正确的是( )
A.SO2(g)+ O2(g) O2(g)  SO3(g)ΔH=-98.3 kJ·mol-1 SO3(g)ΔH=-98.3 kJ·mol-1 |
B.2SO2(g)+O2(g)  2SO3(l)ΔH=-196.6 kJ·mol-1 2SO3(l)ΔH=-196.6 kJ·mol-1 |
C.SO2(g)+ O2(g) O2(g)  SO3(g)ΔH=-78.64 kJ·mol-1 SO3(g)ΔH=-78.64 kJ·mol-1 |
D.2SO2(g)+O2(g)  2SO3(g)ΔH=+196.6 kJ·mol-1 2SO3(g)ΔH=+196.6 kJ·mol-1 |
氯原子对O3分解有催化作用:O3+Cl=ClO+O2 ΔH1,ClO+O=Cl+O2 ΔH2,大气臭氧层的分解反应是:O3+O=2O2 ΔH,该反应的能量变化示意图如图所示,下列叙述中,正确的是( )
| A.反应O3+O=2O2的ΔH=E1-E3 |
| B.反应O3+O=2O2的ΔH=E2-E3 |
| C.O3+O=2O2是吸热反应 |
| D.ΔH=ΔH1+ΔH2 |
通常人们把拆开1 mol某化学键所吸收的能量或形成1 mol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知
| 化学健 | H-H | Cl-Cl | H-Cl |
| 键能 | 436 kJ·mol-1 | 243 kJ·mol-1 | 431 kJ·mol-1 |
则下列热化学方程式不正确的是( )
A.
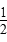 H2(g)+
H2(g)+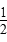 Cl2(g)=HCl(g)ΔH=-91.5 kJ·mol-1
Cl2(g)=HCl(g)ΔH=-91.5 kJ·mol-1B.H2(g)+Cl2(g)=2HCl(g)ΔH=-183 kJ·mol-1
C.
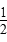 H2(g)+
H2(g)+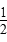 Cl2(g)=HCl(g)ΔH=91.5 kJ·mol-1
Cl2(g)=HCl(g)ΔH=91.5 kJ·mol-1D.2HCl(g)=H2(g)+Cl2(g)ΔH=183 kJ·mol-1
下列说法或表示方法正确的是( )
| A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由“C(石墨)=C(金刚石) ΔH=1.9 kJ·mol” 可知,金刚石比石墨稳定 |
| C.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-285.8 kJ/mol |
| D.在稀溶液中:H++OH-=H2O ΔH=-57.3 kJ·mol ,若将含1 mol H2SO4与含2 mol NaOH的溶液混合,放出的热量等于114.6 kJ |
如图为某反应的焓变示意图,下列有关该反应的说法中正确的是( )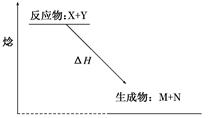
| A.ΔH>0 |
| B.X能量一定高于M |
| C.该反应为放热反应 |
| D.该反应一定不必加热就可以发生 |
在生产和生活中,人们广泛利用着化学反应释放的能量。下列说法正确的是( )
| A.物质发生化学变化并不一定都伴随着能量变化 |
| B.用实验方法和理论方法研究反应热的化学称为热化学 |
| C.有能量变化的都是化学变化 |
| D.任何反应中的能量变化都表现为热量变化 |
某种优质燃油由甲、乙两种有机物混合而成,甲、乙两种物质含有C、H、O三种元素中的两种或三种。已知甲、乙及CO、H2的燃烧热如下:
| 物质 | 甲 | 乙 | CO | H2 |
| 燃烧热/kJ/mol | 1 366 | 5 518 | 283 | 286 |
取甲、乙按不同比例混合的燃油23 g,在足量的O2中燃烧时,放出的热量Q与混合物中乙的物质的量分数x的关系如图所示。试求:
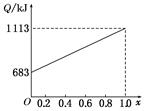
(1)甲、乙的相对分子质量为:Mr(甲)= ,Mr(乙)= 。
(2)1 mol由甲、乙以等物质的量混合而成的燃油在一定量的O2中燃烧,放出热量2 876 kJ,则反应中生成CO mol。
在25℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为( )
| A.-488.3 kJ/mol | B.+488.3 kJ/mol |
| C.-191 kJ/mol | D.+191 kJ/mol |
下列关于热化学反应的描述中正确的是( )
| A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3) kJ/mol |
| B.碳与二氧化碳的反应既是吸热反应,又是化合反应 |
| C.热化学方程式中化学计量数可表示分子个数 |
| D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
已知:①H2(g)+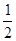 O2(g)=H2O(g)
O2(g)=H2O(g) 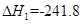 kJ·mol-1,② C(s)+
kJ·mol-1,② C(s)+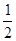 O2(g)="CO(g)"
O2(g)="CO(g)" 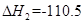 kJ·mol-1。由此可知焦炭与水蒸气反应的热化学方程式为:C(s)+H2O(g)=CO(g)+H2(g)
kJ·mol-1。由此可知焦炭与水蒸气反应的热化学方程式为:C(s)+H2O(g)=CO(g)+H2(g)  ,则
,则 为
为
| A.+131.3 kJ·mol-1 | B.-131.3 kJ·mol-1 |
| C.+352.3 kJ·mol-1 | D.-352.3 kJ·mol-1 |