下列有关热化学方程式的叙述正确的是( )
A.已知C(石墨,s) C(金刚石,s);△H>0,则金刚石比石墨稳定 C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| B.已知C(s)+O2(g)=CO2(g);△H1和C(s)+1/2O2(g)=CO(g);△H2,则△H1>△H2 |
| C.101kPa时,2H2(g)+O2(g)=2H2O(l);△H=-5716kJ/mol,则氢气的燃烧热为285.8kJ/mol |
| D.含20.0gNaOH的稀溶液与稀盐酸完全中和时放出28.7kJ的热量,则该反应的热化学方程式为: NaOH(aq)+HCl(aq)="NaCl(aq)+" H2O(1);△H="+57.4" kJ/mol |
下列反应属于吸热反应的是
| A.石灰石在高温下的分解反应 | B.生石灰和水的反应 |
| C.盐酸与氢氧化钠溶液的反应 | D.木炭在氧气中燃烧 |
下列说法正确的是:
A.在100℃、101kPa条件下,液态水的气化热为40. 69 kJ·mol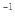 ,则 ,则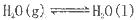  |
B.已知MgCO3的Ksp=6.82×10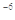 ,则所有含有固体MgCO3的溶液中,都有 ,则所有含有固体MgCO3的溶液中,都有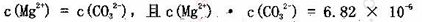 |
C.己知: 则可以计算出反应 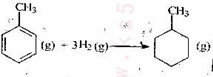  |
D.常温下,在0.10mol 的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的PH减小 的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的PH减小 |
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25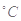 时:
时: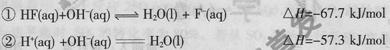
在20Ml0.lmol/L的氢氟酸中滴加0.lmol/L的NaOH V mL,下列说法正确的是
A.氢氟酸的电离方程式及热效应可表示为: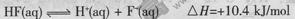 |
B.当V="20" mL时,溶液中: |
C.当V="20" mL时,溶液中: |
D.当v>0时,溶液中一定存在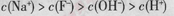 |
下列关于反应热的说法正确的是
| A.当△H为“一”时,表示该反应为吸热反应 |
B.已知C(s)+ O2(g) O2(g) CO(g)的反应热为l10.5kJ/mol,说明碳的燃烧热为110.5kJ/mol CO(g)的反应热为l10.5kJ/mol,说明碳的燃烧热为110.5kJ/mol |
| C.反应热的大小取决于反应物所具有总能量和生成物所具有总能量的相对大小 |
| D.反应热不但与反应体系的始态和终点状态有关,而且与反应的途径也有关 |
下列说法或表示方法中正确的是( )
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.由C(金刚石)→C(石墨)ΔH= -1.9KJ/mol 可知,金刚石比石墨稳定 |
| C.由2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1可知,H2的燃烧热为-571.6 kJ·mol-1 |
| D.稀溶液中:H+(aq)+OH—(aq)=H2O(l) ΔH= —53.7KJ/mol ,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于57.3KJ |
反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
| A.1molA与1molB充分反应后,能量变化为ΔE |
| B.加入催化剂后,反应加快,ΔE减小 |
| C.反应物的总键能小于生成物的总键能 |
| D.反应达到平衡时,升高温度,A的转化率增大 |
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:
下列说法正确的是( )
| A.1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ |
| B.1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 |
| C.通常情况下,N2(g)和O2(g)混合能直接生成NO |
| D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |


 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 升温至t2
升温至t2