原子个数相同、核外电子数相同的分子(离子)的空间构型相同。以下微粒为三角锥形的是
| A.NH4+ | B.H3O+ | C.H2S | D.CH4 |
物质的变化需要改变微粒之间的相互作用,所克服的作用属于同种类型的是
| A.Br2(l)和I2(s)分别受热气化 | B.NaBr和HI分别在水中电离 |
| C.硅和铁分别受热熔化 | D.氯化氢和蔗糖分别溶解于水 |
有关化学键和晶体的说法中正确的是
| A.离子键的本质是静电作用,因此只能存在于由阴、阳离子构成的物质中 |
| B.共价键的本质是共用电子对,因此必须由成键的两原子各提供一个电子形成 |
| C.分子晶体的基本微粒是分子,因此分子晶体中只存在分子间作用力 |
| D.原子晶体由于是空间网状结构,因此只能由碳、硅两元素构成 |
下列物质中,含有共价键的是
| A.MgCl2 | B.CH4 | C.Na2O | D.KBr |
1996年诺贝尔化学奖授予斯莫利等三位化学家,以表彰他们发现富勒烯(C60),开辟了化学研究的新领域。富勒烯(C60)由于具有空心的类似足球形状的结构,也称为足球烯。对于下列有关C60的说法中正确的是
| A.C60在一定条件下可以与CuO发生置换反应 |
| B.C60的摩尔质量是720 |
| C.金刚石、石墨和足球烯(C60)三者和足量氧气反应的最终产物不同 |
| D.金刚石、石墨和足球烯(C60)的性质完全相同 |
下列观点正确的是( )
| A.构成单质分子的微粒一定含有共价键 |
| B.在氧化钠中,只存在氧离子和钠离子的静电吸引作用 |
| C.某化合物熔融态能导电,该化合物中一定有离子键 |
| D.Na2O和Na2O2所含化学键类型完全相同 |
三氟化氮(NF3)在微电子工业中有重要用途,它在潮湿的空气中与水蒸气反应的产物有:HF、NO和HNO3。则下列说法正确的是
| A.NF3分子中含有非极性共价键 |
| B.NF3在空气中泄漏时不易被察觉 |
| C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |
| D.反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
下列说法错误的是( )
| A.对羟基苯甲酸的沸点比邻羟基苯甲酸高,冰中既存在范德华力,又存在氢键 |
| B.简单立方是非密置层三维堆积形成的,面心立方是由密置层三维堆积形成的 |
| C.所有共价键都有方向性,形成氢键的三个相关原子可以不在直线上 |
| D.金属晶体的导电、导热性都与自由电子有关,离子晶体在一定条件下可以导电 |
有关CH2=CH-C≡N分子的说法正确的是( )
A.3个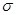 键,2个π键 键,2个π键 | B.5个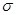 键,3个π键 键,3个π键 |
C.6个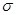 键,2个π键 键,2个π键 | D.6个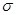 键,3个π键 键,3个π键 |
下列有关作用力的说法正确的是( )
| A.金属键、离子键、分子间作用力都没有方向性和饱和性 |
| B.键能、金属的原子化热、晶格能分别可以衡量氢键、金属键、离子键的强弱 |
| C.离子键、金属键、氢键、范德华力本质上都是静电作用 |
| D.乙酸、丙醇、丙酮的沸点都比丁烷高是因为前三者分子间都存在氢键 |