下列性质中,可以证明某化合物内一定存在离子键的是( )
| A.可溶于水 | B.有较高的熔点 | C.水溶液能导电 | D.熔融状态能导电 |
医学上在对抗癌物质的研究中发现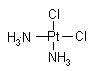 具有抗癌作用,而
具有抗癌作用,而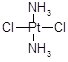 没抗癌作用。对此下列叙述正确的是( )
没抗癌作用。对此下列叙述正确的是( )
| A.两者互为同分异构体,都是以Pt原子为中心的四面体结构 |
| B.两者互为同分异构体,都是以Pt原子为中心的平面结构 |
| C.两者为同一物质,都是以Pt原子为中心的四面体结构 |
| D.两者为同一物质,都是以Pt原子为中心的平面结构 |
三氟化硼(BF3)是一种无色气体,用于制造火箭的高能燃料。已知BF3是非极性分子,下列描述正确的是
| A.BF3分子呈三角锥形 | B.BF3沸点低于BCl3 |
| C.B-F键键能低于B-Cl键 | D.F-B-F间的夹角为109°28′ |
2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体片段结构如图所示。又发现从N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是:
| A.该晶体中含有非极性共价键 |
| B.含N5+离子的化合物中既有离子键又有共价键 |
| C.高聚氮与N2、N3、N5、N5+、N60互为同素异形体 |
| D.这种固体的可能潜在应用是烈性炸药或高能材料 |
二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H2O2相似,熔点为193 K,沸点为411K,遇水很容易反应,产生的气体能使品红褪色,S2C12可由干燥的氯气通入熔融的硫中制得。下列有关说法不正确的是 ( )
| A.S2C12晶体中不存在离子键 |
| B.S2C12分子中各原子均达到8电子稳定结构 |
| C.S2C12在液态下不能导电 |
| D.S2C12与水反应后生成的气体通入石蕊试液中,现象是溶液先变红后褪色 |
已知某碳纳米管为单、双键交替共轭结构,电子传输效果很好,可用作导电材料。现有1根由180个碳原子构成的碳纳米管,若要将这根C180的碳纳米管完全氢化形成C180H180,则放出的热量约为(已知1mol碳碳双键氢化时约放热120kJ)( )
| A.1.79×10-20 kJ | B.3.59×10-20 kJ | C.1.08×104 kJ | D.2.16×104 kJ |
硫的卤化物(S2X2)是广泛用于橡胶工业的硫化剂,S2C12分子结构如图所示。遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2C12+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是( )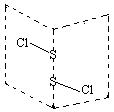
| A.稳定性S2C12>S2Br2 |
| B.反应中,生成1molSO2,转移电子为3mol |
| C.分子中同时含有极性键和非极性键且各原子都满足8电子稳定结构 |
| D.因为S-Cl键能比S-Br键能大,S2C12沸点比S2Br2高 |
在预防甲型H1N1流感疫情时,防疫部门使用了含氯类消毒剂,其中的氯胺是一种长效缓释有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的4—5倍,下列有关氯胺(NH2Cl)的说法一定不正确的是( )
| A.氯胺水解产物为NH2OH(羟氨)和HCl |
| B.氯胺的消毒原理与漂白粉相似 |
| C.氯胺中氯的化合价为+1 |
D.氯胺的电子式为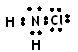 |
下列物质中,既含有极性键,又含有非极性键的是( )
| A.苯(C6H6) | B.CO2 | C.Na2O2 | D.NH4Cl |
随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。 下列有关说法中,正确的是
| A.N5+ 离子中含有36个电子 |
| B.H2与H3属于同素异形体 |
| C.C60720 |
| D.O2与O4属于同位素 |