具有下列电子排布的原子中最难形成离子键的是( )。
| A.1s22s22p2 | B.1s22s22p5 |
| C.1s22s22p63s2 | D.1s22s22p63s1 |
下列元素的原子在形成不同物质时,既能形成离子键,又能形成极性键和非极性键的是( )。
| A.Na | B.Mg | C.Ne | D.Cl |
下列物质中的离子键最强的是( )。
| A.KCl | B.CaCl2 | C.MgO | D.Na2O |
下列用电子式表示形成过程正确的是 ( )。
| A.H∶H+··············―→2H········ |
B. |
C.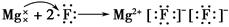 |
D. |
在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是( )。
| A.sp,范德华力 | B.sp2,范德华力 |
| C.sp2,氢键 | D.sp3,氢键 |
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )。
A.NH4Cl NH3↑+HCl↑ NH3↑+HCl↑ |
| B.NH3+CO2+H2O=NH4HCO3 |
| C.2NaOH+Cl2=NaCl+NaClO+H2O |
| D.2Na2O2+2CO2=2Na2CO3+O2 |
有五种元素X、Y、Z、Q、T。X原子的M层上有两个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )。
| A.元素Y和Q可形成一种化合物Y2O3 |
| B.T和Z各有一种单质的空间构型为正四面体形 |
| C.X和Q结合生成的化合物为离子化合物 |
| D.ZO2是极性键构成的非极性分子 |
下列说法中正确的是( )。
| A.ABn型分子中,若中心原子没有孤对电子,则ABn为空间对称结构,属于非极性分子 |
| B.NH3、H2O、CH4分子的几何构型均为三角锥形 |
| C.NH3、H2O、CH4分子中的N、O、C原子均是采取sp2杂化的 |
| D.配合物[Cu(H2O)4]SO4中,中心离子是Cu2+,配位体是SO42-,配位数是1 |
下列有关共价键的叙述中,不正确的是( )。
| A.某原子跟其他原子形成共价键时,其共价键数一定等于该元素原子的价电子数 |
| B.水分子内氧原子结合的电子数已经达到饱和,故不能再结合其他氢原子 |
| C.非金属元素原子之间形成的化合物也可能是离子化合物 |
| D.所有简单离子的核电荷数与其核外电子数一定不相等 |