在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是( )
| A.2Na2O2+2H2O=4NaOH+O2↑ |
| B.Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ |
| C.Cl2+H2O=HClO+HCl |
| D.CaC2+2H2O―→Ca(OH)2+C2H2↑ |
三氯化磷分子的空间构型是三角锥形而不是平面正三角形,下列关于三氯化磷分子空间构型的叙述,不正确的是( )
| A.PCl3分子中的三个共价键的键长、键角都相等 |
| B.PCl3分子中的P—Cl键属于极性共价键 |
| C.PCl3分子中三个共价键的键能均相等 |
| D.PCl3是非极性分子 |
以下有关杂化轨道的说法中错误的是( )
| A.ⅠA族元素成键时不可能有杂化轨道 |
| B.杂化轨道既可能形成σ键,也可能形成π键 |
| C.孤对电子有可能参加杂化 |
| D.s轨道和p轨道杂化不可能有sp4出现 |
关于化学键的叙述中,正确的是
| A.离子化合物可能含共价键 | B.共价化合物可能含离子键 |
| C.离子化合物中只含离子键 | D.离子化合物中一定含有金属离子 |
物质之间发生反应时,一定发生变化的是( )。
| A.颜色 | B.状态 | C.化学键 | D.原子核 |
下列各分子中,所有原子都满足最外层8电子稳定结构的是( )。
| A.H2O | B.BF3 | C.CCl4 | D.PCl5 |
下列叙述正确的是( )。
| A.O2分子间存在着非极性共价键 |
| B.CO2分子内存在着极性共价键 |
| C.SO3与H2O反应的产物是离子化合物 |
| D.盐酸中含有H+和Cl-,故HCl为离子化合物 |
(双选)下列含有共价键的化合物是( )。
| A.HI | B.NaOH | C.Br2 | D.NaCl |
下列反应过程中,同时有离子键、极性共价键和非极性共价键断裂和形成的反应是( )。
A.NH4Cl NH3↑+HCl↑ NH3↑+HCl↑ |
B.NH3+CO2+H2O NH4HCO3 NH4HCO3 |
C.2NaOH+Cl2 NaCl+NaClO+H2O NaCl+NaClO+H2O |
D.2Na2O2+2CO2 2Na2CO3+O2 2Na2CO3+O2 |
下列共价化合物的电子式正确的是( )。
A.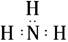 (NH3) (NH3) | B.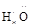 ∶∶ ∶∶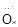 H(H2O2) H(H2O2) |
C.∶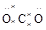 ∶(CO2) ∶(CO2) | D.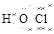 (HClO) (HClO) |