X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g ? L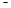 1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是( )
1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是( )
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由Y、Z、M三种元素形成的化合物一定只有共价键 |
下列离子中,所带电荷数与该离子的核外电子层数相等的是:( )
| A.Mg2+ | B.Al3+ | C.Be2+ | D.H+ |
短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是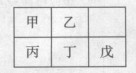
| A.原子半径:丙<丁<戊 |
| B.元素金属性:甲>丙 |
| C.氢氧化物碱性:丙<丁<戊 |
| D.丙的最高价氧化物水化物与戊的最高价氧化物水化物能发生反应 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如右图所示,其中X所处的周期序数与族序数相等。下列说法错误的是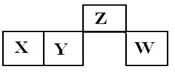
| A.Z的氧化物与W的氧化物的化学键类型相同 |
| B.X、Z的氧化物都能溶于氢氧化钠和稀硫酸溶液中 |
| C.最高价氧化物对应水化物稀溶液的氧化性:W<Z |
| D.Y原子的半径比W原子的半径大 |
下列说法正确的是
| A.Na的原子结构示意图 |
| B.多电子原子中,在离核较远区域运动的电子能量较低 |
| C.非金属元素组成的化合物中可能有共价键和离子键 |
| D.HF、HCl、HBr、HI的热稳定性和还原性依次增强 |
X、Y、Z、W均为短周期元素,其中X、Y、Z在周期表中的相对位置如下图所示。Y是短周期主族元素中原子半径最大的元素,W的最高正化合价与最低负化合价的代数和为0,下列说法中不正确的是
| X | | |
| Y | | Z |
A.W的氧化物可以用于制造太阳能电池
B.最高价氧化物对应水化物的碱性Y比X强
C.可以用电解法制备Z单质
D.Y和Z的最高价氧化物对应水化物之间可以相互反应
几种短周期元素的原子半径及某些化合价见下表,下列说法正确的是( )
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | –1 | –2 | +4、–4 | +7、–1 | +5、–3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
B.A、H、J的离子半径由大到小顺序是A>J>H
C.G元素的单质不存在同素异形体
D.I在DB2中燃烧生成两种化合物
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为11;Y、
Z在同一周期;Z原子最外层电子数是X原子内层电子数的2倍,也是Y原子最外层电子数的2倍。下列说法中,正确的是( )
| A.离子半径:Y>X | B.气态氢化物的稳定性:Z>X |
| C.Y的氧化物中含有离子键 | D.Z的氧化物对应的水化物是弱碱 |
短周期元素X、Y、Z和W的原子序数依次增大。X原子的S能级电子总数是P能级电子总数的2倍,Y与X同主族,Z和W原子中未成对电子数之比为2∶1。下列说法错误的是( )
| A.XW4为非极性分子 |
| B.Y、Z、W的最高价氧化物的水化物酸性强弱顺序是Y<Z<W |
| C.X、Y的氢化物由固态转化为气态时,克服相同的作用力 |
| D.XW4、YW4、ZW2分子中的中心原子均为sp杂化 |
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,能层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是( )
| A.Z与Y形成的化合物可作为耐高温材料 |
| B.WY2能与碱反应,但不能与任何酸反应 |
| C.原子半径按X、Y、Z、R、W的顺序依次增大 |
| D.熔沸点:X2R>X2Y |