W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是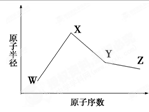
| A.对应简单离子半径X<W |
| B.对应气态氢化物的稳定性Y<Z |
| C.化合物XZW既含离子键也含共价键 |
| D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |
下列说法中,正确的是( )
| A.ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| B.ⅥA族元素的氢化物中,最稳定的氢化物常温时为无色液体 |
| C.某主族元素X的气态氢化物化学式为HX,则其最高正价为+7价 |
| D.金属元素的原子只有还原性,金属阳离子只有氧化性 |
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是( )
| A.Y元素最高价氧化物对应的水化物化学式为H2YO4 |
| B.原子半径由大到小的顺序为:Z>Y>W |
| C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
| D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1∶2 |
元素的原子结构决定其性质和在周期表中的位置,下列有关结构和性质的说法中,正确的是( )
| A.形成离子键的阴阳离子间只存在静电吸引力 |
| B.元素周期表中,第三周期最右端的元素原子得电子能力最强 |
| C.最易失去的电子能量最高 |
| D.目前使用的元素周期表中最长的周期含有36种元素 |
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是
| A.Y元素最高价氧化物对应的水化物化学式H2YO4 |
| B.原子半径由大到小的顺序为:Z>Y> W |
| C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
| D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1︰2 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z为地壳中含量最高的金属元素。下列说法正确的是
| | | | | | | X |
| Y | | Z | | | | W |
A.工业上电解ZW3饱和溶液冶炼金属Z
B.元素X的最高正价与W的最高正价相同
C.简单离子半径的大小顺序:r(Y+)>r(X—)
D.Y、W的最高价氧化物的水化物均能溶解金属Z
已知X、Y、Z、W、T是短周期中原子序数依次增大的5种主族元素。其中Y和X两种元素可以组成1:1、1:2、1:3、1:4等多种化合物; Z原子最外层电子数是次外层电子数的3倍,W与X同主族,W与T形成的化合物WT是厨房必需的调味品。下列说法正确的是( )
| A.原子半径: T> W > Z > Y |
| B.W与T的单质可通过电解饱和的WT水溶液获得 |
| C.Z与W形成的两种化合物中化学键类型完全相同 |
| D.元素X、Z与T可形成多种酸 |
下列有关结构和性质的说法中不正确的是 ( )
| A.元素周期表中从ⅢB族到ⅡB族十个纵行的元素都是金属元素 |
| B.碱性:NaOH > NH3·H2O ,所以元素的金属性:Na > N |
| C.同周期第ⅡA族与第ⅢA族的元素原子序数之差不一定为1 |
| D.第ⅦA族元素从上到下,其氢化物的稳定性逐渐减弱 |
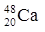 轰击
轰击 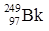 ,生成了6个拥有117个质子的新原子,其中的5个原子有176个中子,1个原子有177个中子。下列有关说法正确的是( )
,生成了6个拥有117个质子的新原子,其中的5个原子有176个中子,1个原子有177个中子。下列有关说法正确的是( )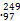 Bk的质量数为97
Bk的质量数为97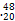 Ca2+的中子数比核外电子数多10
Ca2+的中子数比核外电子数多10