下图是元素周期表的一部分,下列说法正确的是( )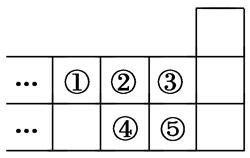
| A.元素①位于第二周期第ⅣA族 |
| B.气态氢化物的稳定性:④<② |
| C.最高价氧化物对应水化物的酸性:⑤<④ |
| D.元素③的最高价是+7 |
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )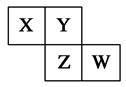
| A.X的气态氢化物比Y的稳定 |
| B.W的最高价氧化物对应水化物的酸性比Z的强 |
| C.Z的非金属性比Y的强 |
| D.X与Y形成的化合物都易溶于水 |
2010年12月3日美国宇航局表示,在地球上发现全新的微生物,它能利用砷代替磷进行新陈代谢,砷含有剧毒。磷一直被认为是生命的6大基本元素,这种细菌的发现或说明可以扩大有机体生存条件及存在可能。下列关于砷和磷两种元素的叙述不正确的是( )
| A.它们的原子最外层电子数相等,元素的最高正化合价都是+5 |
| B.氮的非金属性比砷强,所以NH3的稳定性大于AsH3 |
| C.因为氮的原子半径比砷的小,所以氮的相对原子质量比砷的相对原子质量小 |
| D.它们都是主族元素 |
下列叙述中正确的是( )
| A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| B.除短周期外,其他周期均有18种元素 |
| C.在同一周期中,ⅠA族比ⅡA族的单质与水反应更剧烈 |
| D.在ⅠA族中,单质的熔、沸点随着原子半径的增大而逐渐升高 |
下列关于化学观或化学研究方法的叙述中,错误的是( )
| A.在化工生产中应遵循“绿色化学”的思想 |
| B.在过渡元素中寻找优良的催化剂 |
| C.在元素周期表的金属和非金属分界线附近寻找半导体材料 |
| D.根据元素周期律,由HClO4可以类推出氟元素也存在最高价氧化物的水化物HFO4 |
已知短周期主族元素X、Y、Z、W、Q的原子序数逐渐增大,其中X和Z、Y和W分别为同主族元素,X元素的原子内层电子数是最外层电子数的一半,W的最高价氧化物对应的水化物是二元强酸,则下列说法中正确的是
| A.五种元素均能形成不同种同素异形体 |
| B.X和Y、W分别可以形成XY2、XW2化合物 |
| C.氢化物稳定性由强到弱的是:Q、W、Z、X |
| D.W形成简单阴离子半径小于Q形成简单阴离子半径 |
主族元素M、R形成的简单离子M2-离子与R+离子的核外电子数之和为20,下列说法正确的是
| A.M原子的质子数一定大于R原子的质子数 |
| B.M可能存在16M、18M两种核素 |
| C.M2-的离子与R+的电子层结构不可能相同 |
| D.两种离子结合形成的化合物中可能含有共价键 |
下列说法错误的是
| A.一定条件下,气体体积大小主要由气体的分子数目决定的 |
| B.有热量变化的过程一定有化学键的断裂与形成 |
| C.通过钠、镁、铝与水反应的实验,可以比较三种单质的金属性强弱 |
| D.轮船外壳连接锌块保护外壳不受腐蚀,是采用了牺牲阳极的阴极保护法 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是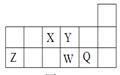
| A.离子半径的大小顺序为:r(W2—)>r(Q—)>r(Y2—)> r(Z3+) |
| B.若存在简单阴离子R2-,则R不一定与Y、W同主族 |
| C.元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键 |
| D.X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应 |
