X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子总数少4,Z原子的最外层电子数是内层电子总数的三倍。下列有关叙述正确的是( )
| A.X、Y、Z三种元素可形成化合物X3YZ4 |
| B.X、Y两元素形成的化合物一定是离子化合物 |
| C.Y、Z两元素形成的化合物熔点较低 |
| D.稳定性:Y的氢化物>Z的氢化物 |
短周期元素甲、乙、丙、丁、戊五种元素在元素周期表中的位置如右图所示,其中戊是同周期中原子半径最小的元素。下列有关判断正确的是( )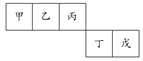
| A.最外层电子数:甲>乙>丙>丁>戊 |
| B.简单离子的离子半径:戊>丁 |
| C.含有丁元素的酸有多种 |
| D.乙的氢化物多种多样,丙、丁、戊的氢化物各有一种 |
X、Y是元素周期表中ⅦA族的两种元素,下列能说明X的非金属性比Y强的是( )。
| A.电子层数:X>Y |
| B.气态氢化物的稳定性:HX<HY |
| C.酸性:HXO4>HYO4 |
| D.能发生置换反应:Y2+2NaX=X2+2NaY |
氧元素是地壳中含量最多的元素。下列说法中正确的是( )
| A.16O2与18O3互为同位素 |
| B.氧元素与其他短周期非金属元素均能形成酸性氧化物 |
| C.氧与钠形成的稳定化合物中,阴、阳离子个数比均为1:2 |
| D.O2变成O3以及16O变成18O的变化均属于化学变化 |
下列对非金属元素(除稀有气体元素外)的相关判断正确的是 ( )
①非金属元素都是主族元素
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以都叫气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价
| A.②⑤ | B.①③⑤ | C.②③④ | D.①⑤ |
下列说法中不正确的是 ( )
| A.同周期元素,随着核电荷数的增加,I1总体上呈现由小到大的变化趋势 |
| B.电离能越大,表示气态时该原子越易失电子 |
| C.元素的电负性越大,表示其原子在化合物中吸引电子能力越强 |
| D.电负性是相对的,所以没有单位 |
下列各组原子中,彼此的化学性质一定相似的是 ( )
| A.P原子:1s2;Q原子:2s2 |
| B.P原子:M能层上有2个电子;Q原子:N能层上有2个电子 |
| C.P原子:2p能级上有1个未成对电子;Q原子:3p能级上也有1个未成对电子 |
| D.P原子:最外层L能层上只有一个空轨道;Q原子:最外层M能层上也只有一个空轨道 |
不能说明元素X的电负性比元素Y的大的是 ( )
| A.与H2化合时X单质比Y单质容易 |
| B.X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 |
| C.X原子的最外层电子数比Y原子的最外层电子数多 |
| D.X单质可以把Y从其氢化物中置换出来 |
在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是 ( )
| A.sp,范德华力 | B.sp2,范德华力 | C.sp2,氢键 | D.sp3,氢键 |