在11 g由D和18O组成的水中,含中子数为(NA表示阿伏加德罗常数)( )。
| A.NA | B.2NA | C.6NA | D.10NA |
下列说法正确的是( )。
| A.所有原子都是由质子、中子和核外电子构成的 |
| B.只要知道粒子的质子数,就一定能确定它是什么元素 |
| C.由于质量数=质子数+中子数,所以,电子是没有质量的 |
| D.分子的质子数等于该分子中各原子质子数之和 |
第四周期某主族元素的原子,它的最外电子层上有2个电子,下列关于此元素的叙述正确的是( )。
| A.原子半径比钾的原子半径大 |
| B.氯化物难溶于水 |
| C.原子半径比镁的原子半径大 |
| D.碳酸盐易溶于水 |
某元素R的气态氢化物的化学式为H2R,则R的最高价氧化物对应水化物化学式是( )。
| A.H2RO3 | B.HRO3 | C.H3RO4 | D.H2RO4 |
(2012北京理综,9)已知33As、35Br位于同一周期。下列关系正确的是( )。
| A.原子半径:As>Cl>P | B.热稳定性:HCl>AsH3>HBr |
| C.还原性:As3->S2->Cl- | D.酸性:H3AsO4>H2SO4>H3PO4 |
下列关于元素周期律的叙述正确的是( )。
| A.随着元素原子序数的递增,原子最外层电子数总是从1到8重复出现 |
| B.随着元素原子序数的递增,原子半径从大到小(稀有气体元素除外)发生周期性变化 |
| C.随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 |
| D.元素性质的周期性变化是指原子核外电子排布的周期性变化、原子半径的周期性变化 |
1941年才第一次制得卤素的第五个成员——砹(At)。下列关于砹及其化合物的性质的预测中,不正确的是( )。
| A.砹与碱金属单质钠能发生反应生成NaAt |
| B.卤素阴离子的还原性强弱次序是:F->Cl->Br->I->At- |
| C.砹的最高价氧化物对应水化物(HAtO4)的酸性比高碘酸(HIO4)的酸性弱 |
| D.砹的气态氢化物(HAt)比溴化氢的稳定性弱 |
(双选)酸根离子R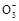 所含电子数比硝酸根离子N
所含电子数比硝酸根离子N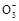 所含的电子数多10个,则下列说法正确的是( )。
所含的电子数多10个,则下列说法正确的是( )。
| A.R原子的电子层数比氮原子的电子层数多1 |
B.酸根离子R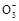 中R的化合价与硝酸根离子N 中R的化合价与硝酸根离子N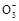 中N的化合价相等 中N的化合价相等 |
C.R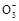 和N 和N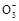 只能被还原,不能被氧化 只能被还原,不能被氧化 |
| D.R原子和氮原子的最外层电子数相同 |
X、Y是元素周期表第ⅦA族中的两种元素。下列叙述中不能说明X的非金属性比Y强的是( )。
| A.X原子的电子层数比Y原子的电子层数少 |
| B.酸性:HXO4>HYO4 |
| C.X的气态氢化物比Y的气态氢化物稳定 |
| D.Y的单质能将X从NaX的溶液中置换出来 |
Mg、Ca、Sr、Ba是按原子序数由小到大的顺序排列的第ⅡA族元素。已知:①Mg(OH)2难溶于水,而Ca(OH)2微溶于水;②MgSO4溶于水,而CaSO4微溶于水。下列推测中,不正确的是( )。
| A.Sr(OH)2溶解于水 | B.SrSO4易溶于水 |
| C.BaSO4不溶于水 | D.Ba(OH)2比Ca(OH)2更易溶于水 |