元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是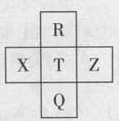
| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q |
| D.最高价氧化物的水化物的酸性:T>Q |
下列性质的递变中,正确的是
| A.O、S、Na的原子半径依次增大 |
| B.HF、NH3、SiH4的稳定性依次增强 |
| C.LiOH、KOH、CsOH的碱性依次增强 |
| D.HCl、HBr、HI的还原性依次减弱 |
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为
| A.HX | B.H2X | C.XH4 | D.XH3 |
根据元素在周期表中的位置判断,下列元素中原子半径最小的是
| A.氧 | B.氟 | C.碳 | D.氮 |
放射性同位素电池采用的放射性同位素主要有90 38Sr等。下列关于90 38Sr的说法正确的是
| A.质子数为90 | B.中子数为38 | C.电子数为52 | D.质量数为90 |
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。若X原子的最外层电子数比其次外层电子数多3个,下列说法不正确的是
| A.原子半径:Z>X>Y |
| B.最高价氧化物对应水化物的酸性:Z>W |
| C.W的单质是制取盐酸的原料之一 |
| D.X、W的氢化物相遇会产生白烟 |
甲、乙两种非金属性质比较:
①甲的单质熔、沸点比乙的低;
②甲单质能氧化乙原子的阴离子;
③最高价氧化物对应的水化物酸性比较,甲比乙的强;
④与金属反应时甲原子得电子的数目比乙多;
⑤甲单质比乙单质容易与氢气化合。
上述项目中能够说明甲比乙的非金属性强的是
| A.①②⑤ | B.③④⑤ | C.②③⑤ | D.②③④⑤ |
在下列元素中,原子半径最小的是
| A.C | B.N | C.O | D.F |
某元素X的气态氢化物的化学式为H2X,则X的最高价氧化物的水化物的化学式为
| A.H2XO3 | B.H2XO4 | C.H3XO4 | D.HXO3 |