实验室中制取下列物质的方案均合理的是
| A.铜和浓硫酸反应,亚硫酸钠和浓硫酸反应均可以制取二氧化硫 |
| B.铜和浓硝酸反应,碳和浓硝酸反应均可以制取二氧化氮 |
| C.向氯化铝溶液中加入过量氨水,或加入过量的氢氧化钠溶液均可制取氢氧化铝 |
| D.向次氯酸钙溶液中通入适量二氧化碳,或通入适量二氧化硫均可制取次氯酸 |
下列定性分析正确的是
| A.Cl2、SO2均能使品红溶液褪色,说明两者均有氧化性 |
| B.SiO2、Al2O3均可和酸与碱反应,说明两者均为两性氧化物 |
| C.浓硫酸、浓硝酸在常温下均能使铁铝钝化,说明两者均有强氧化性 |
| D.钠、铁的金属性均比铜的强,说明两者均可以从硫酸铜溶液中置换出单质铜 |
下列根据实验操作和现象所得出的结论不正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里出现凝胶 | 酸性:盐酸>硅酸 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
| C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁不与浓硫酸反应 |
| D | 向某溶液中先滴加KSCN溶液,再滴加少量氯水 | 先无明显现象,后溶液变成血红色 | 溶液中含有Fe2+,没有Fe3+ |
下列物质转化在给定条件下不能实现的是( )
①Si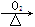 SiO2
SiO2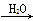 H2SiO3;②S
H2SiO3;②S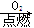 SO3
SO3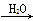 H2SO4;③C
H2SO4;③C CO2
CO2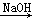 Na2CO3
Na2CO3
④MgCl2溶液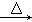 MgCl2·6H2O
MgCl2·6H2O Mg;⑤Na
Mg;⑤Na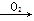 Na2O2
Na2O2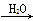 NaOH
NaOH
| A.①②③ | B.①②④ | C.①②③④ | D.①②③④⑤ |
下列有关物质的性质与应用相对应的是( )
| A.氢氟酸具有弱酸性,可用于雕刻玻璃 |
| B.Na2O2具有强氧化性,可用作自来水的消毒剂 |
| C.氯化铁溶液能氧化铜单质,可用于制作印刷电路板 |
| D.SO2具有漂白性,可使酸性高锰酸钾溶液褪色 |
下列有关物质性质的应用不正确的是
| A.浓H2SO4具有吸水性,可用来干燥氨气 |
| B.Na2CO3溶液具有碱性,可用于除器皿表面油污 |
| C.锂质量轻、比能量大,金属锂用作电池负极材料 |
| D.ClO2具有强氧化性,可用于自来水的消毒杀菌 |
根据下列物质的合理性质,判断其应用不正确的是
| A.Al2O3熔点很高,可用于制作耐高温材料 |
| B.二氧化硅具有半导体性能,可以制成光电池 |
| C.次氯酸钠具有强氧化性,可用于配制消毒液 |
| D.明矾水解产生具有吸附性的胶体粒子,可作漂白剂 |
下列各组描述正确的是
| A.化工生产要遵守三原则:充分利用原料、充分利用能量、保护环境。①燃烧时使用沸腾炉②制盐酸时将氯气在氢气中燃烧③制硫酸时使用热交换器这3种化工生产分别符合以上某原则 |
| B.① 用燃烧的方法鉴别甲烷、乙烯和乙炔②用酒精萃取溴水中的溴③ 用水鉴别硝酸铵和氢氧化钠固体④用互滴法鉴别Na2CO3、盐酸、BaCl2、NaCl四种溶液以上均能达到实验目的 |
| C.①用硫粉覆盖地下撒有的汞②金属钠着火用泡沫灭火器或干粉灭火器扑灭③用热碱溶液洗去试管内壁的硫④用湿的红色石蕊试纸检验氨气是否集满以上操作均合理 |
| D.①过氧化氢:火箭燃料②碳酸氢钠:食品发酵剂③钠:制氢氧化钠④硫酸:制蓄电池以上物质的用途均合理 |
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 选项 | 叙述I | 叙述II |
| A | NH4Cl加热有类似升华现象 | 用加热法除去NaCl中的NH4Cl |
| B | Fe的金属活动性大于Cu | 用FeCl3溶液可以腐蚀Cu |
| C | 水解程度:NaHCO3<Na2CO3 | 溶解度:Na2CO3>NaHCO3 |
| D | HNO3具有不稳定性 | 浓HNO3应保存在棕色试剂瓶中 |
下列推断正确的是
| A.SiO2是酸性氧化物,不能与任何酸反应 |
| B.Na2CO3、NaHCO3都是盐,都能与CaCl2溶液反应 |
| C.CO、NO都是大气污染气体,在空气中都能稳定存在 |
| D.将SO2通入Ba(ClO)2的溶液中,生成BaSO4沉淀 |