化学美无处不在,下图是物质间发生化学反应的颜色变化,其中X是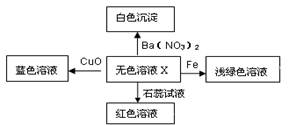
| A.稀盐酸 | B.稀硫酸 | C.硫酸钠溶液 | D.碳酸钠溶液 |
下列实验现象不能说明相关结论的是
| A.铜与浓硫酸共热,产生使石蕊溶液变红的气体,说明浓硫酸具有酸性 |
| B.将金属钠投入冷水中,钠熔为小球,说明钠与水的反应为放热反应且钠的熔点低 |
| C.向AgCl浊液中滴加Na2S溶液,白色沉淀变成黑色,说明AgCl的溶解平衡正向移动 |
| D.向Al(OH)3沉淀中滴加NaOH溶液或盐酸,沉淀均消失,说明Al(OH)3是两性氢氧化物 |
下列事实所对应的方程式不正确的是
| A.盛放氢氧化钠溶液的试剂瓶不能用玻璃塞:SiO2+2NaOH=Na2SiO3+H2O |
B.高温下铁与水蒸气反应生成保护膜:2Fe+6H2O(g) 2Fe(OH)3+3H2 2Fe(OH)3+3H2 |
| C.工业制取漂粉精:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O |
D.实验室制取氨气:2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+ 2H2O CaCl2+2NH3↑+ 2H2O |
下列各组物质充分反应后过滤,将滤液加热、蒸干至质量不变,最终不能得到纯净物的是
| A.向漂白粉溶液中通入过量CO2 |
| B.向带有氧化膜的铝片中加入盐酸 |
| C.向含1 mol Ca(HCO3)2的溶液中加入1 mol Na2O2 |
| D.向含1 mol KAl(SO4)2的溶液中加入2 mol Ba(OH)2 |
下列实验不能达到目的的是
| A.向Na2SiO3溶液中滴加酚酞,溶液变红,证明Na2SiO3发生了水解反应 |
| B.向HClO溶液中通入SO2,生成H2SO4,证明H2SO4的酸性比HClO强 |
| C.铝箔在酒精灯火焰上加热,铝箔熔化但不滴落,证明氧化铝熔点高于铝 |
| D.将饱和氯水滴到蓝色石蕊试纸上,试纸先变红后褪色,证明氯水有漂白性 |
下列有关物质性质的应用不正确的是
| A.浓硫酸具有吸水性,可用来干燥氯气 |
| B.明矾水解得氢氧化铝胶体,可用作净水剂 |
| C.液氨汽化时要吸收大量的热,可用作制冷剂 |
| D.二氧化硅不与强酸反应,可用玻璃容器盛放氢氟酸 |
下列物质的转化在给定条件下不能实现的是
A.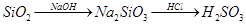 |
B.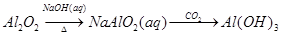 |
C.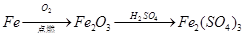 |
D.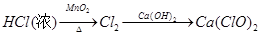 |
下列图中的实验方案,能达到实验目的的是
| | A | B | C | D |
| 实验方案 | 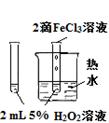 |  | 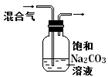 | 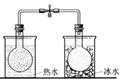 将NO2球浸泡在冰水和热水中 |
| 实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 比较HCl、H2CO3和H2SiO3的酸性强弱 | 除去CO2气体中混有的SO2 | 探究温度对平衡 2NO2  N2O4的影响 N2O4的影响 |
下列实验的现象与对应结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下将铁片分别放在浓硝酸和稀硝酸中 | 在浓硝酸中无明显变化,稀硝酸中有气泡 | 稀硝酸的氧化性比浓硝酸强 |
| B | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| C | 将水蒸气通过灼热的铁粉 | 铁粉变成红棕色粉末 | 铁与水在高温下发生反应 |
| D | 常温下将Al片放入浓硫酸中 | 无明显变化 | Al与浓硫酸不反应 |
下列推断正确的是
| A.CO、NO、NO2都是大气污染的气体,在空气中都能稳定存在 |
| B.Na2O、Na2O2组成元素相同,两化合物中阴阳离子个数比也相同 |
| C.SiO2是酸性氧化物,只能与碱反应而不能与酸反应 |
| D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红 |