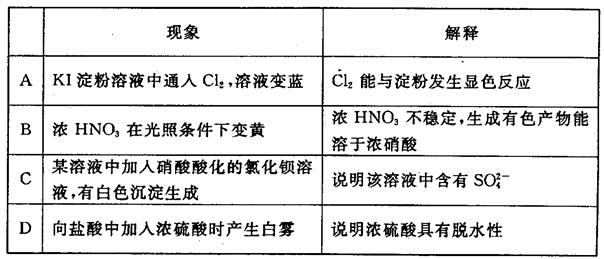
题目内容
下列事实所对应的方程式不正确的是
| A.盛放氢氧化钠溶液的试剂瓶不能用玻璃塞:SiO2+2NaOH=Na2SiO3+H2O |
B.高温下铁与水蒸气反应生成保护膜:2Fe+6H2O(g) 2Fe(OH)3+3H2 2Fe(OH)3+3H2 |
| C.工业制取漂粉精:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O |
D.实验室制取氨气:2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+ 2H2O CaCl2+2NH3↑+ 2H2O |
B
解析试题分析:A、SiO2为酸性氧化物,与NaOH反应生成Na2SiO3和H2O,化学方程式为:SiO2+2NaOH=Na2SiO3+H2O,正确;B、高温下铁与水蒸气反应生成保护膜,氧化膜的成分为Fe3O4,错误;C、工业制取漂粉精,Cl2与Ca(OH)2反应生成CaCl2、Ca(ClO)2、H2O,方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,正确;D、实验室用NH4Cl与Ca(OH)2反应制取NH3,化学方程式为:2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+ 2H2O,正确。
CaCl2+2NH3↑+ 2H2O,正确。
考点:本题考查化学方程式的书写。

练习册系列答案
相关题目
下列各选项的变化中,不能通过置换反应实现的是
| A.CO2→MgO | B.Fe3O4→H2O | C.FeCl3→CuCl2 | D.MnO2→Al2O3 |
蒸干并灼烧下列物质的水溶液,仍能得到该物质的是
| A.碳酸钠 | B.碳酸氢钠 | C.硫酸亚铁 | D.氯化铝 |
下列图中的实验方案,能达到实验目的的是
| | A | B | C | D |
| 实验方案 | 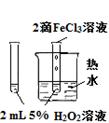 |  | 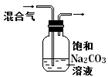 | 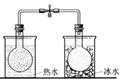 将NO2球浸泡在冰水和热水中 |
| 实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 比较HCl、H2CO3和H2SiO3的酸性强弱 | 除去CO2气体中混有的SO2 | 探究温度对平衡 2NO2  N2O4的影响 N2O4的影响 |
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是 ( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | H2O2、SO2都能使酸性高锰酸钾褪色 | 前者表现出还原性后者表现出漂白性 |
| B | 纯银器表面在空气中渐渐变暗 | 发生了化学腐蚀 |
| C | SiO2能与氢氟酸及碱反应 | SiO2是两性氧化物 |
| D | 反应物比例不同可导致产物不同 | Na与O2反应可能生成Na2O,也可能生成Na2O2 |
下列化合物不能由两种单质直接化合而成的是( )。
| A.FeCl2 | B.Na2S | C.FeCl3 | D.SO2 |
下列实验中,溶液颜色有明显变化的是( )
| A.少量明矾溶液加入到过量NaOH溶液中 |
| B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 |
| C.少量Na2O2固体加入到过量NaHSO3溶液中 |
| D.往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3溶液 |
下列说法正确的是
| A.铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应 |
| B.硅在电子工业中是最重要的半导体材料,广泛用于制作光导纤维 |
| C.二氧化硫是一种有毒气体,所以不能用于杀菌消毒 |
| D.氨很容易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂 |