下列化学实验有关的叙述正确的是( )
| A.某无色溶液中滴加BaCl2溶液出现白色沉淀,说明该无色溶液中一定含有SO42— |
| B.向2.0 mL浓度均为0.1 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1AgNO3溶液,振荡,生成黄色沉淀,说明Ksp(AgI)比Ksp(AgCl)大 |
| C.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜熔点高于铝 |
| D.SO2、Cl2都能使品红试液褪色,其原理是相同的 |
下列实验“操作和现象”与“结论”对应关系正确的是( )
| | 操作和现象 | 结论 |
| A | 向装有Fe(NO3)2溶液的试管中加入稀硫酸,在管口观察到红棕色气体 | HNO3分解成了NO2 |
| B | 向淀粉溶液中加入质量分数为20%的硫酸,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 甲烷和氯气混合后在光照下,颜色逐渐褪去 | 甲烷和氯气发生了化合反应 |
| D | 向饱和Na2CO3中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )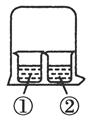
| | ①中的物质 | ②中的物质 | 预测①中的现象 |
| A | 淀粉-KI溶液 | 浓溴水 | 无明显变化 |
| B | 石蕊溶液 | 硫酸 | 无明显变化 |
| C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
| D | AgNO3溶液 | 浓盐酸 | 有白色沉淀 |
下列事实与结论(或推论)均正确的是( )
| A.将浓氨水加到盛有AgCl固体的试管中,AgCl固体完全溶解,则所得溶液中c(Ag+)·c(Cl-)>Ksp(AgCl) |
| B.物质的量之比为1?2的Na2O2和NaHCO3的固体混合物,在密闭容器中充分加热反应后,残留的固体是Na2CO3 |
| C.向FeBr2溶液中通入少量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变为红色;那么向FeI2溶液中通入少量的氯气,也会出现同样的现象 |
| D.将某混合气体通入品红溶液中,溶液不褪色,该气体中无Cl2 |
下列对有关物质性质的分析正确的是( )
| A.Na久置于空气中,可以和空气中的有关物质反应,最终生成NaHCO3 |
| B.在高温下用氢气还原MgCl2可制取金属镁 |
| C.实验测得NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性:CH3COOH>H2CO3 |
| D.N2的化学性质通常非常稳定,但在放电条件下可以与O2反应生成NO2 |
下列物质的转化在给定条件下能实现的是( )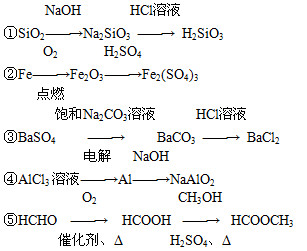
| A.①④⑤ | B.②③④ | C.②④⑤ | D.①③⑤ |
向下列溶液滴加稀硫酸,生成白色沉淀,继续滴加稀硫酸,沉淀又溶解的是
| A.Na2SiO3 | B.BaCl2 | C.CaCl2 | D.NaAlO2 |
下列说法正确的是( )
| A.电解、电镀、电化学腐蚀都需要通电才可进行 |
| B.Al、Fe、Cu三者对应的氧化物均为碱性氧化物 |
| C.浓H2SO4和新制氯水分别滴在pH试纸上均会出现先变红后褪色的现象 |
| D.从石油中得到汽油,可采用分馏的方法 |
下列有关物质性质的描述和该性质的应用均正确的是( )
| A.氨气具有氧化性,用浓氨水检验氯气管道是否泄漏 |
| B.氢氟酸具有强酸性,用氢氟酸蚀刻玻璃 |
| C.二氧化硫具有还原性,用二氧化硫水溶液吸收溴蒸气 |
| D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
下列有关物质的性质或应用的叙述正确的是( )
| A.MgO的熔点很高,可用于制作耐高温材料 |
| B.Na2O2是酸性氧化物,因其强氧化性可用于杀菌消毒 |
| C.氨气是一种碱性气体,可用P2O5或无水氯化钙干燥 |
| D.SO2和Cl2都能使品红溶液褪色,将两者等体积混合可使它们的漂白能力增强 |