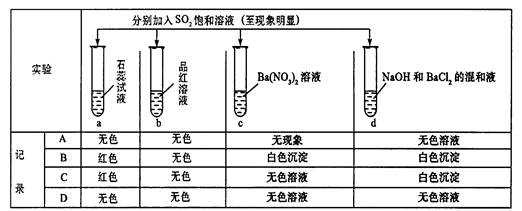
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A.向NaHCO3固体中加入新制的氯水,有无色气泡产生(H+) |
| B.新制氯水使红色布条褪色(HCl) |
| C.将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl-) |
| D.向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,溶液呈红色(Cl2) |
向含有NaBr 、KI的混合溶液中通入过量的Cl2充分反应。将溶液蒸干并灼烧,最后剩余的固体物质是( )
| A.NaCl 和KI | B.NaCl、KCl和I2 | C.KCl和NaBr | D.KCl和NaCl |
漂白粉在空气中放置易失效的主要原因是( )
| A.Ca(ClO)2不稳定,易分解 | B.Ca(ClO)2易吸收水分而潮解 |
| C.Ca(ClO)2跟空气中的水和CO2反应 | D.Ca(ClO)2跟空气中的CO2反应 |
多数自来水是采用氯气消毒的,为检验自来水中Cl–的存在,最好选用下列物质中的 ( )
| A.石蕊试液 | B.四氯化碳 | C.氢氧化钠溶液 | D.硝酸银溶液 |
在氯水中存在许多分子和离子,它们在不同的反应中表现各自的性质,下列的实验和结论一致且正确的是
| A.加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2的存在 |
| B.溶液呈浅黄绿色,且有刺激性气味,说明溶液中有Cl2的存在 |
| C.先加入盐酸酸化,再加入AgNO3溶液产生白色沉淀,说明氯水中有Cl-的存在 |
| D.加入NaOH溶液,氯水浅黄绿色消失,说明溶液中有HClO分子的存在 |
下列物质不能用单质与氯气直接反应来制取的是
| A.氯化铜 | B.氯化镁 | C.氯化亚铁 | D.氯化氢 |
单晶硅是制作电子集成电路的基础材料。科学家预计,到2014年一个电脑芯片上将会集成100亿个晶体管,其功能远比我们想象的要大的多,这对硅的纯度要求很高。用化学方法可制得高纯度硅,其化学方程式为 :
①SiO2 + 2C Si + 2CO
Si + 2CO
②Si + 2Cl2 SiCl4
SiCl4
③SiCl4 + 2H2 Si + 4HCl
Si + 4HCl
其中,反应①和③属于
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应o |
硅被誉为无机非金属材料的主角。下列物品用到硅单质的是
| A.陶瓷餐具 | B.石英钟表 | C.计算机芯片 | D.光导纤维 |
不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | HCl | CO2 | 石灰水 |
| ③ | CO2 | SO2 | Ba(NO3)2 |
| ④ | NO2 | SO2 | BaCl2 |
| ⑤ | CO2 | NH3 | CaCl2 |