实验室常用全是磨砂接口的曲颈甑制取HNO3(如图),反应的化学方程式为:NaNO3+H2SO4 NaHSO4+HNO3↑用曲颈甑是因为HNO3
NaHSO4+HNO3↑用曲颈甑是因为HNO3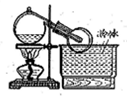
| A.会腐蚀橡胶 | B.易挥发 |
| C.易分解 | D.是强电解质 |
某同学利用下列装置进行浓硫酸和铜反应并验证二氧化硫的性质。按如图实验装置连接仪器和放置药品。加热浓硫酸约1分钟后撤去酒精灯,将铜丝插入液面,反应一段时间后拔出。实验结束后会看到两个试管的液体底部均有少量的白色固体。下列对该实验的现象分析或推断正确的是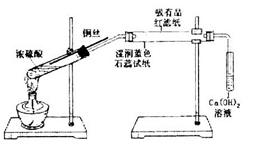
| A.湿润的蓝色石蕊试纸先变红后褪色 |
| B.左边试管出现的白色固体是由于浓硫酸的脱水性所致 |
| C.从该实验的描述中可以体会出铜与浓硫酸的反应是一个放热反应 |
| D.本实验体现了二氧化硫的酸性、漂白性和弱氧化性 |
下列说法正确的是
| A.自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片 |
| B.硅酸钠的水溶液俗称水玻璃,可用作木材防腐剂 |
| C.水泥、玻璃、水晶都是硅酸盐制品 |
| D.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
如图所示,大试管里充满某混合气体,置于光亮处,将滴管里的水挤入大试管后,烧杯中的水会进入大试管,大试管里的气体可能是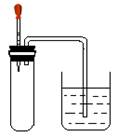
①N2、H2;②CO、O2; ③NO2、O2;④CH4、Cl2
| A.①或③ | B.②或④ | C.①或③或④ | D.③或④ |
下列有关H2SO4的说法中正确的是
| A.将过量的Zn投入一定量的浓H2SO4中,最终生成的气体只有SO2 |
| B.向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 |
| C.运输保存浓硫酸的槽罐车一旦泄露后应立即用大量水冲洗 |
| D.向5 mL 18 mol·L-1的硫酸中加入足量铜片并加热使其充分反应,生成0.045 mol SO2 |
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种。若该气体为无色气体,且通过品红溶液后,品红溶液褪色,剩余气体与空气接触时,很快变为红棕色。下列判断正确的是
| A.肯定只有NO | B.肯定有SO2和NO2 |
| C.可能有Cl2和O2 | D.肯定没有Cl2、O2和NO2 |
硅及其化合物在材料领域中应用广泛。下列叙述中不正确的是( )
| A.硅单质可用来制造太阳能电池 |
| B.装碱性溶液的玻璃试剂瓶不能用玻璃塞 |
| C.二氧化硅是制造光导纤维的材料 |
| D.二氧化硅属于酸性氧化物,不能与任何酸反应 |
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是 ( )
| A.肯定有SO2和NO | B.肯定只有NO |
| C.可能有Cl2和O2 | D.肯定没有Cl2、NO2,可能有O2 |
检验SO2气体中是否混有CO2气体,可采用的方法是( )
| A.通过品红溶液 |
| B.通过澄清石灰水 |
| C.先通过氢氧化钠溶液,再通过澄清石灰水 |
| D.先通过酸性高锰酸钾溶液,再通过澄清石灰水 |
关于非金属元素Si、N、S、Cl的叙述,正确的是( )
| A.通常情况下,它们的单质均为气体 |
| B.它们在自然界中都存在游离态形式 |
| C.它们都有对应的含氧酸 |
| D.每种元素都只有一种氧化物 |